LETYBO 50 unités, poudre pour solution injectable
Classe médicamenteuse
Relaxants musculaires, Autres relaxants musculaires, Agents à action périphérique, | Code ATC : M03AX01
Composition
Chaque flacon contient 50 unités de toxine botulinique de type A produit par Clostridium botulinum.
Après reconstitution, chaque 0,1 mL de solution contient 4 unités.
Indications thérapeutiques
Letybo est indiqué dans la correction temporaire de l’apparence des rides verticales intersourcilières modérées à sévères chez l’adulte de moins de 75 ans observées lors du froncement maximal des sourcils (rides glabellaires), lorsque la sévérité des rides du haut du visage entraîne un retentissement psychologique important.
Posologie et mode d'administration
Letybo doit être administré exclusivement par des médecins possédant les qualifications et l’expertise appropriées pour ce traitement et pour l’utilisation du matériel requis.
Posologie
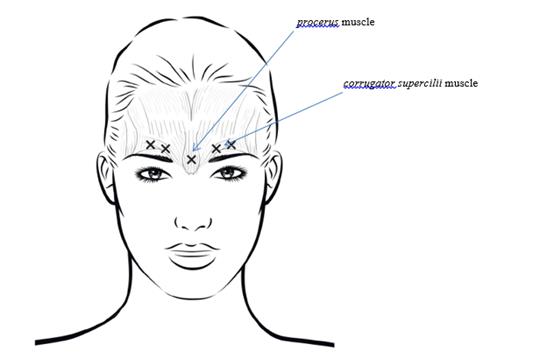
La dose recommandée est un total de 20 unités réparties en cinq injections de 4 unités (0,1 mL) chacune : 2 injections dans chaque muscle corrugator supercilii et 1 injection dans le muscle procerus.
Les unités de toxine botulinique ne sont pas interchangeables d’un produit à l’autre.
Les doses recommandées diffèrent des autres préparations de toxine botulinique.
L’intervalle entre les traitements doit être d’au moins trois mois.
En l’absence d’effets indésirables consécutifs à une séance de traitement, il est possible d’entamer une nouvelle séance après un délai d’au moins trois mois.
En cas d’échec du traitement un mois après une première séance, c’est-à-dire en l’absence d’amélioration significative par rapport à la situation initiale, les approches suivantes peuvent être envisagées :
- L’analyse des causes de l’échec, par exemple l’injection dans les mauvais muscles, une technique d’injection inappropriée, la formation d’anticorps neutralisant la toxine ou un dosage insuffisant.
- La réévaluation de la pertinence du traitement par toxine botulinique de type A.
L’efficacité et la sécurité des injections répétées de Letybo au-delà d’une période de 12 mois n’ont pas été évaluées.
Populations particulières
Sujets âgées
Il n’existe pas de données cliniques concernant l’utilisation de Letybo chez les patients de plus de 75 ans. Aucun ajustement spécifique de la dose n’est nécessaire pour l’utilisation chez les personnes âgées de plus de 65 ans (voir rubrique 5.1).
Population pédiatrique
Il n’y a pas d’utilisation justifiée de Letybo dans la population pédiatrique (voir rubrique 5.1).
Mode d’administration
Voie intramusculaire.
Après reconstitution, Letybo ne doit être utilisé que pour une seule séance d’injection(s) par patient.
Pour les instructions concernant la dilution, l’utilisation, la manipulation et l’élimination des flacons, voir rubrique 6.6.
Les injections intramusculaires doivent être réalisées à l’aide d’une seringue stérile du type utilisé pour l’insuline ou la tuberculine, avec une capacité de 1 mL, des graduations de 0,01 mL et une aiguille de calibre 30 à 31 G.
Aspirer dans la seringue stérile 0,5 mL de la solution dûment reconstituée et expulser toute bulle d’air présente dans le cylindre. L’aiguille utilisée pour reconstituer le médicament doit être retirée et remplacée pour l’administration.
Veiller à ce que Letybo ne soit pas injecté dans un vaisseau sanguin.
Afin de réduire le risque de blépharoptose, éviter les injections à proximité du muscle levator palpebrae superioris, en particulier chez les patients présentant des puissants complexes abaisseurs des sourcils. Lors de l’injection dans deux sites pour chaque muscle corrugator supercilii, réaliser la première injection juste au-dessus du bord médial des sourcils. La seconde injection sera pratiquée à environ 1 cm au-dessus du bord supra-orbitaire (limites osseuses rigides palpables au-dessus de la marge haute de la paupière supérieure), au point de rencontre des lignes médianes des sourcils. Le site d’injection pour le muscle procerus se situe juste au-dessus de la ligne médiane de l’arête nasale, à l’endroit où se forment les rides horizontales entre les extrémités médiales des sourcils. Lors de l’administration dans les extrémités médiales des muscles corrugator supercilii et sur les lignes médianes des sourcils, les sites d’injection doivent être éloignés d’au moins 1 cm du bord supra-orbitaire (limites osseuses rigides palpables au-dessus de la marge haute de la paupière supérieure).
![]()
![]()
Lors de l’administration, agir avec prudence pour éviter toute injection intravasculaire. Avant l’injection, il est possible de placer fermement le pouce ou l’index sous le bord orbitaire pour éviter l’épanchement du médicament dans cette zone. Orienter l’aiguille vers le haut et médialement.
Voie d'administration
intramusculaire
Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
Troubles généralisés de l’activité musculaire (par exemple, myasthénie grave, syndrome de Lambert-Eaton, sclérose latérale amyotrophique).
Présence d’une infection ou d’une inflammation aiguë aux sites d’injection proposés.
Mise en garde et précautions d'emploi
Généralités
Avant toute administration de Letybo, il importe de comprendre l’anatomie des muscles et des structures vasculaires et nerveuses environnantes dans la région glabellaire, ainsi que toute altération anatomique liée à des interventions chirurgicales antérieures. Éviter l’injection dans des structures anatomiques vulnérables.
Agir avec prudence si Letybo est utilisé alors que le muscle ciblé présente une faiblesse ou une atrophie excessive.
Il existe un risque de ptosis après le traitement. Voir les instructions d’administration à la rubrique 4.2 pour limiter cette éventualité.
Événements liés à la procédure
Après le traitement par d’autres toxines botuliniques, une douleur et/ou une anxiété liée à l’aiguille ont donné lieu à des réactions vasovagales, notamment à une hypotension symptomatique transitoire et à une syncope.
Troubles neuromusculaires préexistants
Les patients atteints de troubles neuromusculaires non reconnus peuvent présenter un risque accru d’effets systémiques cliniquement significatifs à l’administration de doses standard de toxine botulinique de type A, notamment une dysphagie sévère et une atteinte respiratoire.
Réactions d’hypersensibilité
Dans de très rares cas, une réaction anaphylactique peut se produire après l’injection de toxine botulinique. Il convient donc d’avoir à disposition de l’épinéphrine (adrénaline) ou toute autre mesure anti-anaphylactique.
Diffusion locale ou à distance des effets de la toxine
Des effets indésirables potentiellement liés à la diffusion de la toxine à distance du site d’administration ont été signalés dans de très rares cas pour la toxine botulinique (voir rubrique 4.8). Les patients recevant des doses thérapeutiques peuvent présenter une faiblesse musculaire excessive.
Les difficultés à avaler et à respirer sont graves et peuvent entraîner la mort. L’injection de Letybo n’est pas recommandée chez les patients présentant des antécédents de dysphagie et d’inhalation.
Les patients doivent être avertis de la nécessité d’une prise en charge médicale immédiate en cas d’apparition de troubles de la déglutition, de troubles de la parole ou de troubles respiratoires.
Formation d’anticorps
L’administration de doses trop rapprochées ou trop élevées peut accroître le risque de formation d’anticorps. La formation d’anticorps peut entraîner l’échec du traitement par toxine botulinique de type A, même dans le cadre d’autres indications.
Troubles hémorragiques
Agir avec prudence lorsque Letybo est utilisé chez des patients présentant des troubles hémorragiques, car l’injection peut générer des contusions.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu’il est essentiellement « sans sodium ».
Traçabilité
Afin d’améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Condition de prescription
prescription réservée aux spécialistes et services OPHTALMOLOGIE
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Non disponible
Présentation : 1 flacon en verre de 5 mL
Prix : non disponible
Taux de remboursement : 0%
Titulaire : CROMA PHARMA (AUTRICHE)