BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO 160 microgrammes/4,5 microgrammes/dose, poudre pour inhalation en récipient unidose
Classe médicamenteuse
médicaments pour les syndromes obstructifs des voies aériennes : adrénergiques, médicaments pour inhalation | code ATC : R03AK07
Composition
Budésonide...................................................................................................... 194,7 microgrammes
Fumarate de formotérol dihydraté......................................................................... 6,1 microgrammes
Pour chaque dose nominale
Budésonide........................................................................................................ 160 microgrammes
Fumarate de formotérol dihydraté......................................................................... 4,5 microgrammes
Pour chaque dose délivrée au travers de l’embout buccal
Excipients à effet notoire : lactose monohydraté (5,4 mg par dose nominale et 4,4 mg par dose délivrée)
Indications thérapeutiques
Asthme
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO est indiqué chez l’adulte et l’adolescent (à partir de l’âge de 12 ans) en traitement continu de l'asthme persistant, dans les situations où l’administration par voie inhalée d’un médicament associant un corticoïde et un bronchodilatateur β2 mimétique de longue durée d’action est justifiée :
- chez les patients insuffisamment contrôlés par une corticothérapie inhalée et la prise d’un bronchodilatateur β2 mimétique de courte durée d’action par voie inhalée à la demande.
- ou
- chez les patients déjà contrôlés par l’administration d’une corticothérapie inhalée associée à un traitement continu par β2 mimétique de longue durée d’action par voie inhalée.
Bronchopneumopathie chronique obstructive (BPCO)
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO est indiqué en traitement symptomatique de la BPCO chez les adultes âgés de 18 ans et plus dont le VEMS (mesuré après administration d’un bronchodilatateur) est inférieur à 70 % de la valeur théorique et ayant des antécédents d’exacerbations malgré un traitement bronchodilatateur continu (voir également la rubrique 4.4).
Posologie et mode d'administration
Voie d’administration : voie inhalée.
Posologie
Asthme
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO ne doit pas être utilisé pour l’initiation d’un traitement antiasthmatique.
La posologie est individuelle. Le dosage de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO sera prescrit en fonction de la sévérité de la maladie. Ceci devra être respecté non seulement lorsque l’association est initiée, mais également lors de l’ajustement de la posologie.
Que ce soit à l’initiation ou pendant les phases d’adaptation du traitement de fond, si les dosages disponibles de l’association fixe de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO ne permettent pas d’ajuster la posologie de chacun des principes actifs en fonction de l’état clinique du patient, β2 mimétique et/ou corticostéroïdes devront être administrés individuellement.
Il convient de toujours rechercher la posologie minimale efficace permettant d'obtenir le contrôle des symptômes.
Le médecin vérifiera régulièrement que le dosage prescrit de budésonide/formotérol est adapté pour un traitement optimal du patient. Lorsque celui-ci est obtenu avec la posologie minimale recommandée, l’administration d’un corticoïde seul pourra être envisagée comme étape suivante dans la recherche du traitement minimal efficace.
S’il est approprié de diminuer la posologie à une dose plus faible ou de prescrire une dose plus importante que celle qui est disponible dans BUDESONIDE/FUMARATE DE FORMOTEROL SANDOZ, il est recommandé de passer à une autre association fixe de budésonide et de fumarate de formotérol contenant une dose plus faible ou plus élevée du corticostéroïde inhalé.
Il existe deux modalités thérapeutiques d’administration de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO :
A. BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO utilisé en traitement continu de fond :
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO est utilisé comme traitement continu de fond et un bronchodilatateur d’action rapide est utilisé séparément pour soulager les symptômes d’asthme.
B. BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO utilisé à la fois en traitement continu de fond et, en cas de besoin, pour soulager les symptômes d’asthme :
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO est utilisé à la fois en traitement continu de fond et, en cas de besoin, en réponse à la survenue de symptômes d’asthme pour les soulager.
A. BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO utilisé en traitement continu de fond :
Il convient d’informer les patients qu’ils doivent avoir en permanence à leur disposition leur bronchodilatateur d’action rapide en traitement de secours pour soulager les symptômes aigus d’asthme.
Posologie préconisée :
Adultes (18 ans et plus) : 1–2 inhalations 2 fois par jour.
Certains patients peuvent nécessiter 4 inhalations 2 fois par jour.
Population pédiatrique:
Adolescents (12-17 ans) : 1–2 inhalations 2 fois par jour.
En pratique courante, lorsque les symptômes ont régressé avec 2 prises quotidiennes, un rythme d'administration de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO en 1 prise par jour peut éventuellement être envisagé dans le cadre de la recherche de la dose minimale efficace si le médecin estime nécessaire de maintenir un traitement par bêta-2 adrénergique longue durée d'action pour le contrôle des symptômes.
Une augmentation de la consommation du bronchodilatateur d'action rapide pour soulager les symptômes aigus d'asthme est le signe d'une déstabilisation de l'asthme et nécessite une réévaluation du traitement.
Enfants de moins de 12 ans : comme il n’existe aucune donnée disponible, BUDESONIDE/ FORMOTEROL SANDOZ n'est pas recommandé chez les enfants de moins de 12 ans.
- B. BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO utilisé à la fois en traitement continu de fond et, en cas de besoin, pour soulager les symptômes d’asthme :
Les patients prennent quotidiennement BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO en traitement continu de fond et utilisent aussi BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO en cas de besoin en réponse à la survenue de symptômes d’asthme pour les soulager.
Les patients devront être informés qu'ils doivent avoir en permanence BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO à leur disposition pour une utilisation en cas de besoin.
L'utilisation de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO en traitement continu de fond et pour soulager les symptômes d’asthme sera envisagée notamment chez des patients :
- ayant un contrôle insuffisant de l’asthme avec recours fréquent aux β2 mimétiques de courte durée d’action inhalés,
- ayant eu des antécédents d’exacerbations d’asthme ayant nécessité une intervention médicalisée.
- Une surveillance médicale attentive des effets indésirables dose-dépendants est nécessaire chez les patients consommant de façon fréquente des doses journalières élevées de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO pour soulager leurs symptômes d’asthme.
Posologie préconisée :
Adultes et adolescents (12 ans et plus) :
La dose recommandée en traitement continu de fond est de 2 inhalations par jour, administrées en deux prises par jour (1 inhalation matin et soir), ou en une prise (2 inhalations le matin ou le soir). Chez certains patients, une dose quotidienne de fond de 2 inhalations deux fois par jour peut être nécessaire.
En cas de besoin, les patients pourront prendre 1 inhalation supplémentaire de BUDESONIDE/ FORMOTEROL SANDOZ pour traiter les symptômes aigus d'asthme. Si les symptômes persistent après quelques minutes, l'inhalation sera renouvelée.
Ne pas prendre plus de 6 inhalations en 1 seule fois.
Une dose totale quotidienne de plus de 8 inhalations n'est généralement pas nécessaire. Toutefois, une dose totale journalière allant jusqu'à 12 inhalations pourra être utilisée sur une période limitée. Il convient de fortement recommander aux patients utilisant plus de 8 inhalations par jour de prendre un avis médical. Leur traitement d'entretien devra être réévalué.
Enfants âgés de moins de 12 ans :
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO n’est pas recommandé pour le traitement continu de fond de l’asthme ni pour le soulagement des symptômes aigus d’asthme.
BRONCHOPNEUMOPATHIE CHRONIQUE OBSTRUCTIVE (BPCO) :
Posologie préconisée
Adultes : 2 inhalations deux fois par jour.
Informations générales
Populations spécifiques :
Sujets âgés : pas de recommandation posologique particulière.
Insuffisance hépatique ou rénale : aucune donnée n'est disponible concernant l'utilisation de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO chez les patients insuffisants hépatiques ou insuffisants rénaux. Compte tenu de l'élimination principalement par métabolisme hépatique du budésonide et du formotérol, une augmentation de l'exposition systémique est attendue chez les patients présentant une cirrhose hépatique sévère.
Mode d’administration
Instructions d’utilisation
Il conviendra de démontrer aux patients comment utiliser l’inhalateur FORSPIRO et une utilisation correcte devra être vérifiée régulièrement.
L’inhalateur contient 60 doses de médicament en poudre dans une bandelette d’aluminium enroulée. Il comporte un compteur de doses qui indique le nombre de doses restant en comptant de 60 à 0. Lorsque les 10 dernières doses sont atteintes les nombres apparaissent sur un fond rouge.
L’inhalateur n’est pas rechargeable - il doit être jeté lorsqu’il est vide et remplacé par un neuf.
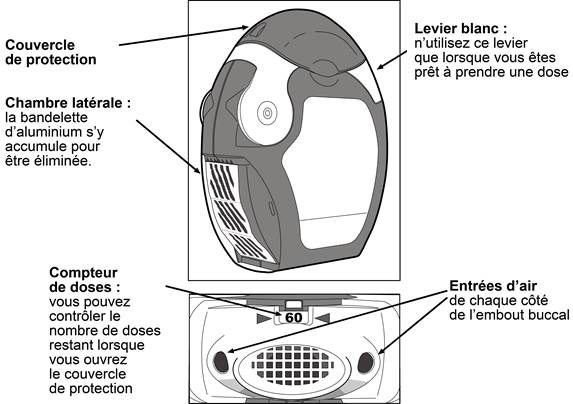
Avant d’utiliser l’inhalateur
- Le volet transparent de la chambre latérale doit être ouvert.
- La bandelette d’aluminium doit être retirée de la chambre latérale en tirant soigneusement toute la longueur de la bandelette contre les « dents » de la chambre latérale comme indiqué ci-dessous. La bandelette ne doit pas être tirée ou tiraillée.
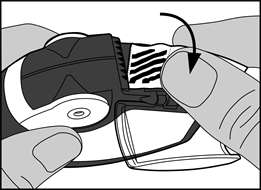
- Le volet de la chambre latérale doit être fermé et la bandelette utilisée doit être jetée.
Note : lorsque l’inhalateur est utilisé, la chambre latérale va se remplir progressivement avec la bandelette utilisée. La bandelette d’aluminium avec les barres noires ne contient pas de médicament. Finalement les sections numérotées de la bandelette vont apparaitre dans la chambre latérale. Il ne doit jamais y avoir plus de 2 sections de la bandelette d’aluminium dans la chambre latérale car elles pourraient boucher l’inhalateur. La bandelette doit être découpée soigneusement comme indiqué ci-dessus et jetée de manière sécurisée.
Utilisation de l’inhalateur
L’inhalateur doit être tenu dans les mains, comme indiqué sur les illustrations.
1. Ouvert
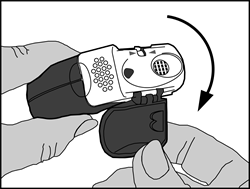
- Le couvercle de protection doit être ouvert vers le bas pour dégager l’embout buccal.
- Le compteur de doses doit être vérifié pour connaître le nombre de doses restantes.
2. Préparation de la dose
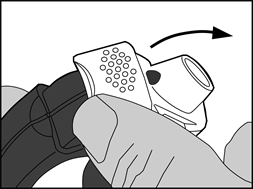
- Le bord du levier blanc doit être soulevé. La chambre latérale doit être fermée.
Remarque : le levier blanc ne doit être actionné que lorsque le patient est prêt à inhaler une dose du médicament. Des doses seront gaspillées si le patient joue avec le levier blanc.
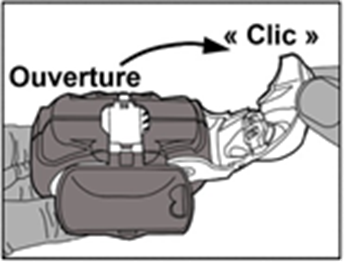
- Ouverture : le levier blanc doit être ouvert entièrement jusqu’au maximum et jusqu’au clic. Cette action déplace une nouvelle dose dans la position avec le numéro au-dessus.
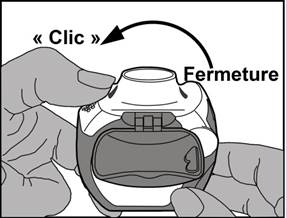
- Fermeture : ensuite, le levier blanc doit être fermé complètement jusqu’à ce qu’il retrouve sa position d’origine en émettant un clic. L’inhalateur est maintenant prêt pour une utilisation immédiate.
3 - Inhalation de la dose
- À distance de l’embout buccal, le patient doit expirer le plus possible sans que cela lui soit inconfortable. Il ne doit jamais expirer directement dans l’inhalateur car cela pourrait affecter la dose.
- L’inhalateur doit être maintenu horizontal avec le couvercle de protection dirigé vers le bas.
- Les lèvres doivent être refermées fermement autour de l’embout buccal.
- Le patient doit inspirer aussi profondément et aussi fort que possible à travers l’inhalateur et non par le nez.
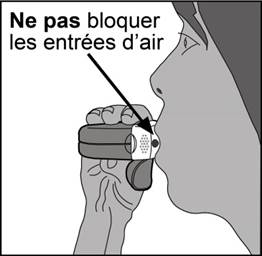
- L’inhalateur doit être retiré de la bouche et le souffle doit être retenu pendant 5 à 10 secondes ou aussi longtemps que possible sans que cela ne soit inconfortable.
- Ensuite le patient doit expirer lentement, mais pas dans l’inhalateur.
- Le couvercle de protection doit être refermé sur l’embout buccal.
- La bouche doit être rincée avec de l’eau qui doit être recrachée ensuite. Cela pourra aider à éviter une infection fongique buccale et un enrouement.
Nettoyage
- L’extérieur de l’embout buccal doit être essuyé avec un tissu propre et sec, si nécessaire.
- L’inhalateur ne doit pas être démonté pour le nettoyer ou pour toute autre raison.
- Les éléments de l’inhalateur ne doivent pas être nettoyés avec de l’eau ou des chiffons humides car l’humidité peut affecter la dose.
- Ne jamais insérer d’aiguilles ou d’objets pointus dans l’embout buccal ou tout autre élément car cela pourrait endommager l’inhalateur.
Voie d'administration
inhalée
Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
Mise en garde et précautions d'emploi
Avant l'arrêt du traitement, les doses devront être diminuées progressivement ; le traitement ne devant pas être arrêté brutalement.
Si le contrôle des symptômes reste insuffisant à la suite du traitement par BUDESONIDE/ FORMOTEROL SANDOZ ou si le patient dépasse les doses maximales recommandées de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO , la conduite thérapeutique devra être réévaluée (voir rubrique 4.2). Une détérioration soudaine ou progressive du contrôle des symptômes d'asthme ou de la BPCO nécessite un avis médical urgent car elle peut annoncer une évolution vers un asthme aigu grave engageant le pronostic vital. Il conviendra alors d'envisager une augmentation de la corticothérapie (avec éventuellement une cure de corticoïdes oraux) et/ou une antibiothérapie en cas d'infection.
Il convient d'informer les patients qu'ils doivent avoir en permanence à leur disposition leur inhalateur de secours : soit BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO (pour les patients asthmatiques utilisant BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO à la fois en traitement d'entretien régulier de l’asthme et pour soulager les symptômes aigus d'asthme), soit un autre médicament bronchodilatateur d'action rapide (pour tous les patients utilisant BUDESONIDE/ FORMOTEROL SANDOZ FORSPIRO uniquement pour le traitement d'entretien régulier de l’asthme).
Il conviendra de rappeler au patient qu'il doit prendre la dose d'entretien de BUDESONIDE/ FORMOTEROL SANDOZ régulièrement en respectant la prescription médicale, même en l'absence de symptômes d'asthme.
L'utilisation de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO en traitement préventif, notamment avant un effort, n'a pas été étudiée. La prise de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO « à la demande » ne doit s'envisager qu'en réponse à la survenue de symptômes d'asthme dans le but de les soulager, mais elle ne doit pas correspondre à une utilisation préventive systématique telle que pour la prévention de l'asthme d'effort. Pour une telle utilisation, il convient d'avoir recours à un médicament contenant un bronchodilatateur d'action rapide seul.
Dès que les symptômes de l'asthme sont bien contrôlés, une diminution progressive de la dose de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO doit être envisagée. Il est important que les patients soient suivis régulièrement lors de la phase de réduction du traitement. La dose minimale efficace de de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO doit être utilisée (voir rubrique 4.2).
Le traitement par BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO ne doit pas être initié pendant une exacerbation, une aggravation significative ou une détérioration aiguë de l'asthme.
Des événements indésirables graves liés à l'asthme et des exacerbations peuvent survenir au cours du traitement par BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO. Il convient d'informer les patients de la nécessité de consulter un médecin tout en poursuivant leur traitement si les symptômes de l'asthme persistent ou s'aggravent.
Aucune étude clinique n'est disponible avec l'association budésonide/formotérol chez les patients présentant une BPCO et un VEMS pré-bronchodilatateur > 50 % de la valeur prédite et un VEMS post-bronchodilatateur < 70 % de la valeur prédite (voir rubrique 5.1).
Comme avec d'autres traitements administrés par voie inhalée, une augmentation des sibilants bronchiques et de la dyspnée juste après l'administration du produit traduit un bronchospasme paradoxal qui doit conduire à l'arrêt immédiat du traitement par BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO. La conduite thérapeutique devra être réévaluée pour envisager si nécessaire les traitements alternatifs. Le bronchospasme paradoxal sera traité immédiatement par un bronchodilatateur inhalé d'action rapide (voir rubrique 4.8).
La corticothérapie inhalée peut entraîner des effets systémiques, en particulier lors de traitements prolongés à fortes doses. La survenue de ces effets est néanmoins beaucoup moins probable avec la corticothérapie inhalée qu'avec la corticothérapie par voie systémique. Les effets systémiques possibles incluent un syndrome de Cushing, un tableau cushingoïde, une inhibition de la fonction surrénalienne, un retard de croissance chez les enfants et les adolescents, une diminution de la densité minérale osseuse, une cataracte et un glaucome et, plus rarement, des troubles psychologiques et comportementaux, notamment hyperactivité psychomotrice, troubles du sommeil, anxiété, dépression ou agressivité (en particulier chez l'enfant) (voir rubrique 4.8).
L'effet potentiel de la corticothérapie sur la densité minérale osseuse, en particulier lors de traitements prolongés à fortes doses, doit être pris en considération chez les patients présentant des facteurs de risque associés d'ostéoporose. Des études à long terme conduites chez des enfants recevant des doses quotidiennes moyennes de 400 µg (dose nominale) ou chez des adultes recevant des doses quotidiennes de 800 µg (dose nominale) de budésonide par voie inhalée n'ont pas montré d'effets significatifs sur la densité minérale osseuse. Il n'y a pas de donnée disponible concernant les effets de doses de budésonide/formotérol plus élevées.
En cas de suspicion d’inhibition de la fonction surrénalienne en relation avec une corticothérapie préalable par voie systémique, une attention particulière sera portée lors de la mise en route d’un traitement par BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO.
L’administration de budésonide par voie inhalée favorise la diminution du recours aux corticoïdes oraux pour le traitement des symptômes de l’asthme, néanmoins les patients traités préalablement par une corticothérapie orale restent à un risque élevé d’insuffisance surrénale pendant longtemps. La récupération peut prendre un temps considérable après l’arrêt de la corticothérapie orale et donc les patients cortico-dépendants passant à un traitement par budésonide en inhalation peuvent garder une insuffisance adrénergique pendant longtemps. Dans ces situations, la fonction surrénalienne doit être surveillée.
Le traitement prolongé par corticoïdes inhalés à fortes doses, notamment à des doses supérieures aux doses recommandées, peut également entraîner une inhibition de la fonction surrénalienne cliniquement significative. Une corticothérapie adaptée de supplémentation devra être envisagée dans les périodes de stress, en cas d'infection sévère ou de chirurgie programmée.
La diminution rapide de la dose de corticoïdes peut entraîner une insuffisance surrénale aiguë. Celle-ci peut se manifester par des symptômes atypiques, tels que : anorexie, douleurs abdominales, perte de poids, fatigue, céphalées, nausées, vomissements, troubles de la conscience, convulsions, hypotension et hypoglycémie.
La corticothérapie systémique et le traitement par budésonide inhalé ne doivent pas être interrompus brutalement.
Lors du relais de la corticothérapie orale par BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO peuvent apparaitre des symptômes évocateurs d'allergie ou d'arthrite tels qu'une rhinite, un eczéma, des myalgies et/ou des arthralgies.
Un traitement adapté sera envisagé. Dans de rares cas, des symptômes tels que fatigue, céphalées, nausées et vomissements peuvent être observés et doivent faire suspecter une insuffisance cortico-surrénalienne. Il peut être nécessaire d’augmenter temporairement la dose de glucocorticoïdes oraux.
Afin de réduire le risque de candidose oropharyngée (voir rubrique 4.8), il sera recommandé aux patients de se rincer la bouche avec de l'eau après chaque prise du traitement d'entretien. En cas de candidose oropharyngée, les patients devront également se rincer la bouche avec de l'eau après les inhalations supplémentaires prises "à la demande".
L'administration concomitante d'itraconazole, de ritonavir ou d'autres inhibiteurs puissants du CYP3A doit être évitée (voir rubrique 4.5). Si cela n'est pas possible, l'intervalle de temps entre l'administration des médicaments doit être aussi long que possible. L'utilisation de BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO à la fois pour le traitement régulier d'entretien et en prises "à la demande" pour traiter les symptômes aigus d'asthme, n'est pas recommandée chez les patients traités par des inhibiteurs puissants du CYP3A.
Une augmentation du risque d'effets indésirables systémiques est attendue avec l'administration concomitante d’inhibiteurs du CYP3A, dont le cobicistat. L'association de budésonide avec des produits contenant du cobicistat doit donc être évitée, sauf si le bénéfice attendu avec la corticothérapie est supérieur au risque d'effets indésirables systémiques des corticoïdes. Dans ce cas, une surveillance accrue des effets indésirables des corticoïdes est nécessaire.
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO doit être administré avec précaution chez les patients présentant les pathologies suivantes: thyrotoxicose, phéochromocytome, diabète sucré, hypokaliémie non traitée, cardiomyopathie obstructive, sténose aortique sous-valvulaire idiopathique, hypertension artérielle sévère, anévrisme ou autres troubles cardiovasculaires sévères, tels que cardiopathie ischémique, tachyarythmies ou insuffisance cardiaque sévère.
La prudence est requise chez les patients présentant un allongement de l'intervalle QTc. Le formotérol peut lui-même provoquer un allongement de l'intervalle QTc.
Le bénéfice de la corticothérapie inhalée et sa posologie devront être réévalués en cas de tuberculose pulmonaire active ou quiescente ou d'infections respiratoires fongiques ou virales.
Des doses élevées d'agonistes des récepteurs β2 adrénergiques peuvent entraîner une hypokaliémie potentiellement grave. L’administration concomitante de bêta-2 adrénergiques avec des médicaments hypokaliémiants ou pouvant potentialiser cet effet, tels que les dérivés xanthiques, les corticoïdes ou les diurétiques, peut induire une augmentation du risque d’hypokaliémie. La prudence est particulièrement recommandée chez les patients ayant un asthme instable et une utilisation variable de bronchodilatateurs "à la demande" pour traiter des symptômes aigus, car le risque associé peut être majoré par l'hypoxémie au cours d'une crise d'asthme ou par toutes les situations susceptibles d'induire une hypokaliémie. Dans ces cas, une surveillance de la kaliémie est recommandée.
Comme avec tous les bêta2 agonistes, des contrôles supplémentaires de la glycémie peuvent être justifiés chez les patients diabétiques.
Troubles visuels
Une perturbation visuelle peut être signalée lors d’une utilisation systémique et topique de corticoïdes. Si un patient présente des symptômes tels qu’une vision trouble ou d'autres troubles visuels, le patient doit être dirigé vers un ophtalmologiste afin d'évaluer les causes possibles, ce qui peut inclure la cataracte, le glaucome ou des maladies rares et des maladies telles que la Choriorétinopathie Séreuse Centrale (CRSC), qui ont été rapportés après utilisation de corticoïdes systémiques et topiques.
BUDESONIDE/FORMOTEROL SANDOZ FORSPIRO contient du lactose monohydraté (4,4 mg/inhalation). Cette quantité ne cause normalement pas de problème chez les patients intolérants au lactose. L’excipient lactose contient de petites quantités de protéines de laits pouvant causer des réactions allergiques.
Population pédiatrique
Il est recommandé de surveiller régulièrement la croissance des enfants recevant des corticoïdes inhalés à long terme. En cas de ralentissement de la croissance, le traitement devra être réévalué en vue de réduire, si possible, la dose du corticoïde inhalé à la dose minimale efficace permettant le maintien du contrôle de l’asthme. Les bénéfices de la corticothérapie et les risques possibles de ralentissement de la croissance doivent être soigneusement évalués. L’avis d’un spécialiste pneumopédiatre peut être requis.
Des données limitées issues d’études cliniques à long terme suggèrent que la plupart des enfants et des adolescents traités par du budésonide inhalé atteindront leur taille adulte prédite. Toutefois, il a été observé un léger ralentissement initial mais transitoire de la croissance (environ 1 cm), généralement pendant la première année de traitement.
Pneumonie chez les patients présentant une BPCO
Une augmentation de l’incidence des cas de pneumonie, ayant ou non nécessité une hospitalisation, a été observée chez les patients présentant une BPCO et recevant une corticothérapie inhalée. Bien que cela ne soit pas formellement démontré dans toutes les études cliniques disponibles, ce risque semble augmenter avec la dose de corticoïde administré.
Les données disponibles ne permettent pas de considérer que le niveau du risque de survenue de pneumonie varie en fonction du corticostéroïde inhalé utilisé.
Il convient de rester vigilant chez les patients présentant une BPCO, les symptômes de pneumonie pouvant s'apparenter aux manifestations cliniques d'une exacerbation de BPCO.
Le tabagisme, un âge avancé, un faible indice de masse corporelle (IMC) ainsi que la sévérité de la BPCO sont des facteurs de risques de survenue de pneumonie.
Condition de prescription
liste I
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Important
Présentation : 2 plaquette(s) OPA : polyamide orienté aluminium PVC-Aluminium de 60 dose(s) avec 2 inhalateur(s) en plastique
Prix : 27.27
Taux de remboursement : 65%
Titulaire : SANDOZ