COSIDIME 20 mg/mL + 5 mg/mL, collyre en solution
Classe médicamenteuse
antiglaucomateux et myotiques, bétabloquants, timolol, associations | code ATC : S01ED51
Composition
Dorzolamide (sous forme de chlorhydrate)............................................................................. 20 mg
Timolol (sous forme de maléate)............................................................................................... 5 mg
Pour 1 mL.
Indications thérapeutiques
Indiqué dans le traitement de l'augmentation de la pression intraoculaire (PIO) chez les patients présentant un glaucome à angle ouvert, ou un glaucome pseudo-exfoliatif, lorsqu'une monothérapie topique par bétabloquant est insuffisante.
Posologie et mode d'administration
Posologie
La posologie est une goutte de COSIDIME collyre en solution deux fois par jour dans le cul-de-sac conjonctival de l'œil ou des yeux affectés.
En cas d'utilisation concomitante d'un autre médicament ophtalmique topique, COSIDIME collyre en solution et l'autre médicament doivent être administrés à au moins 10 minutes d'intervalle.
COSIDIME collyre en solution est une solution stérile qui ne contient pas d'agent de conservation. La solution du flacon multi-dose peut être utilisée pendant au plus 28 jours après la première ouverture pour une administration dans l'œil ou les yeux affectés.
Les patients doivent être informés qu'ils doivent se laver les mains avant l'utilisation et d'éviter de mettre en contact l'embout du flacon avec l'œil ou les structures environnantes afin d'éviter une lésion oculaire.
Les patients doivent aussi être informés que les solutions ophtalmiques incorrectement manipulées peuvent devenir contaminées par des bactéries communes, connues pour provoquer des infections oculaires. L'utilisation de solutions contaminées peut provoquer des lésions graves de l'œil, susceptibles d'entraîner une perte de vision.
Population pédiatrique
L'efficacité n'a pas été établie chez les patients pédiatriques.
La sécurité chez les patients pédiatriques de moins de 2 ans n'a pas été établie. (Voir rubrique 5.1 pour plus d'informations sur la sécurité chez les patients pédiatriques d'âge ≥ 2 ans et < 6 ans).
Mode d'administration
Avant l'instillation du collyre
- Les patients doivent être informés qu'ils doivent se laver les mains avant d'ouvrir le flacon.
- Les patients doivent également être informés qu'ils ne doivent pas utiliser ce médicament si la fermeture de sécurité scellée du col du flacon a été rompue avant la première utilisation.
- Lors de la première utilisation, avant l'instillation d'une goutte dans l'œil, le patient doit s'entraîner à utiliser le flacon en le comprimant lentement pour émettre une goutte en dehors de l'œil.
- Quand le patient se sent confiant pour administrer une goutte à la fois, il doit adopter une position la plus confortable pour l'instillation des gouttes (assis, allongé sur le dos ou debout devant un miroir).
Instillation
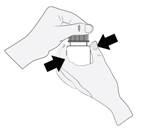
1. Le flacon doit être tenu juste sous le bouchon et le bouchon doit être pivoté pour ouvrir le flacon. Afin d'éviter une contamination de la solution, il faut éviter tout contact de l'embout du flacon avec toute surface.
|
|
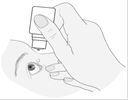
2. Le patient doit basculer la tête en arrière et tenir le flacon au-dessus de l'œil.
3. Le patient doit tirer la paupière inférieure vers le bas et regarder vers le haut. La partie moyenne du flacon doit être délicatement comprimée et une goutte doit tomber sur l'œil du patient. Quelques secondes peuvent s'écouler entre la compression du flacon et la sortie de la goutte. Le flacon ne doit pas être comprimé trop fortement.
Les patients doivent être informés qu'ils doivent demander conseil à leur médecin, pharmacien ou infirmier/ère s'ils ont des doutes sur la méthode d'administration du médicament.
|
|
4. Le patient doit cligner deux ou trois fois les paupières pour répartir la goutte sur l'œil.
|
|
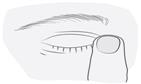
5. Après l'instillation de COSIDIME, le patient devra appuyer son doigt dans le coin de l'œil, à côté du nez, pendant environ deux minutes. Le passage systémique est réduit par une occlusion nasolacrymale ou la fermeture des paupières pendant 2 minutes. Cette technique peut permettre une diminution des effets indésirables systémiques et une augmentation de l’efficacité locale.
|
|
6. Si nécessaire, répéter les étapes 2 à 5 pour l'administration sur l'autre œil. Le patient doit être clairement informé si un seul œil nécessite un traitement et le cas échéant, quel œil est affecté.
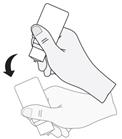
7. Après chaque utilisation et avant de remettre en place le capuchon, le flacon doit être secoué une fois vers le bas, sans toucher l'embout, pour éliminer toute solution résiduelle de l'embout. C'est nécessaire pour permettre l'administration des gouttes ultérieurement.
|
|
8. À la fin des 28 jours d'utilisation du médicament, il peut subsister du COSIDIME dans le flacon. Le patient ne doit pas utiliser le reste de médicament contenu dans le flacon après le déroulement du traitement. Les patients ne doivent pas utiliser le collyre pendant plus de 28 jours après la première ouverture du flacon.
Voie d'administration
ophtalmique
Contre-indications
COSIDIME collyre en solution est contre-indiqué chez des patients qui présentent les conditions suivantes :
- maladie réactive des voies respiratoires, notamment asthme ou antécédent d'asthme bronchique, ou broncho-pneumopathie obstructive chronique sévère
- bradycardie sinusale, syndrome sinusal, bloc sino-auriculaire, bloc auriculo-ventriculaire de deuxième ou troisième degré non contrôlé par un stimulateur cardiaque, insuffisance cardiaque avérée, choc cardiogénique
- insuffisance rénale sévère (ClCr < 30 mL/mn) ou acidose hyperchlorémique
- hypersensibilité à une ou aux deux substances actives ou à un des excipients mentionnés dans la rubrique 6.1
Les contre-indications ci-dessus sont basées sur les composants et ne sont pas spécifiques de l'association.
Mise en garde et précautions d'emploi
Réactions cardiovasculaires/ respiratoires
Comme d'autres médicaments ophtalmiques topiques, le timolol est l'objet d'une absorption systémique. Comme le composant timolol est bêta-adrénergique, les mêmes types d'effets cardiovasculaires, pulmonaires et autres effets indésirables que ceux observés avec les bétabloquants systémiques peuvent survenir. L'incidence des effets indésirables systémiques après une instillation ophtalmique topique est plus faible que lors d'administration systémique. Pour la réduction de l'absorption systémique, voir rubrique 4.2.
Affections cardiaques
Les patients avec maladies cardiovasculaires (par exemple coronaropathie, angor de Prinzmetal et insuffisance cardiaque) et sous traitement hypotenseur par bétabloquants doivent être soigneusement évalués, et un traitement avec d'autres substances actives doit être envisagé. Les patients avec maladie cardiovasculaire doivent être surveillés pour la détection des signes d'aggravation de ces maladies et l'apparition d'effets secondaires.
Du fait de leur effet négatif sur le temps de conduction, les bétabloquants doivent être administrés avec prudence chez les patients avec bloc cardiaque du premier degré.
Affections vasculaires
Les patients avec troubles/anomalies circulatoires périphériques sévères (par exemple formes sévères de la maladie ou du syndrome de Raynaud) doivent être traités avec prudence.
Affections respiratoires
Des réactions respiratoires, y compris le décès par bronchospasme chez des patients asthmatiques, ont été rapportées après administration de bétabloquants ophtalmiques.
COSIDIME collyre en solution doit être utilisé avec prudence chez les patients avec broncho-pneumopathie chronique obstructive (BPCO) légère à modérée, et seulement si le bénéfice potentiel est supérieur au risque potentiel.
Insuffisance hépatique
Ce médicament n'a pas été étudié chez des patients avec insuffisance hépatique et doit donc être utilisé avec prudence chez ces patients.
Immunologie et hypersensibilité
Comme pour tout médicament ophtalmique topique, ce médicament peut entraîner une absorption systémique. Le dorzolamide contient un groupe sulfonamide, également présent dans les sulfamides. Par conséquent, les mêmes types d'effets indésirables que ceux observés avec l'administration systémique de sulfamides peuvent survenir suite à une administration topique, notamment des réactions sévères comme un syndrome de Stevens-Johnson ou une nécrolyse épidermique toxique. L'utilisation de ce médicament doit être arrêtée en cas d'apparition de signes de réactions graves ou d'hypersensibilité.
Des réactions indésirables oculaires, similaires à celles observées avec les collyres à base de chlorhydrate de dorzolamide, ont été observées avec ce médicament. Si de telles réactions surviennent, il convient d'envisager l'arrêt de l'utilisation de COSIDIME collyre en solution.
Les patients sous bétabloquants qui ont des antécédents d'atopie ou de réactions anaphylactiques sévères à divers allergènes peuvent être plus réactifs à des contacts répétés à de tels allergènes et ne pas répondre aux doses habituelles d'adrénaline utilisées pour traiter les réactions anaphylactiques
Traitement concomitant
L'effet sur la pression intraoculaire ou les effets systémiques bétabloquants connus peuvent être potentialisés lorsque le timolol est administré à des patients déjà traités par un bétabloquant systémique. La réponse de ces patients doit être étroitement surveillée. L'utilisation de deux agents bêta-adrénergiques topiques est déconseillée (voir rubrique 4.5).
L'utilisation du dorzolamide et d'inhibiteurs de l'anhydrase carbonique oraux est déconseillée.
Arrêt du traitement
Comme avec les bétabloquants systémiques, s'il est nécessaire d'arrêter le timolol ophtalmique chez des patients avec coronaropathie, le traitement doit être arrêté progressivement.
Autres effets des bétabloquants
Hypoglycémie/ diabète
Les bétabloquants doivent être administrés avec prudence chez les patients sujets à une hypoglycémie spontanée ou chez les patients atteints d'un diabète instable, parce que les bétabloquants peuvent masquer les signes et symptômes d'hypoglycémie aiguë.
Les bétabloquants peuvent également masquer les signes d'hyperthyroïdie. Un sevrage brutal du traitement par bétabloquants peut précipiter une aggravation des symptômes.
Affections de la cornée
Les bétabloquants ophtalmiques peuvent induire une sécheresse oculaire. Les patients qui présentent des affections de la cornée doivent être traités avec prudence.
Anesthésie chirurgicale
Les préparations ophtalmiques contenant des bétabloquants peuvent bloquer les effets systémiques des bêta-agonistes, par exemple de l'adrénaline. L'anesthésiste doit être informé lorsque le patient est traité par le timolol.
Le traitement par bétabloquants peut aggraver les symptômes d'une myasthénie grave.
Autres effets de l'inhibition de l'anhydrase carbonique
Le traitement oral par inhibiteurs de l'anhydrase carbonique a été associé à une lithiase urinaire résultant de déséquilibres acidobasiques, particulièrement chez des patients avec antécédents de calculs rénaux. Bien qu'on n'ait pas observé de déséquilibres acidobasiques avec le dorzolamide/timolol (formulation avec conservateur), des cas de lithiases urinaires ont été rarement rapportés. Comme l'association dorzolamide/timolol sans conservateur contient un inhibiteur de l'anhydrase carbonique topique à absorption systémique, les patients avec antécédents de calculs rénaux peuvent donc présenter un risque accru de lithiases urinaires lors de l'utilisation de ce médicament.
Autres
La prise en charge de patients avec glaucome aigu par fermeture de l'angle nécessite des interventions thérapeutiques en plus des médicaments hypotenseurs. Ce médicament n'a pas été étudié chez les patients atteints de glaucome aigu par fermeture de l'angle.
Des cas d'œdème cornéen et de décompensation irréversible de la cornée ont été décrits lors de traitement par dorzolamide chez des patients présentant une altération chronique préexistante de la cornée et/ou ayant des antécédents de chirurgie intraoculaire. Les patients avec faible nombre de cellules endothéliales présentent un plus grand risque de développer un œdème cornéen. Il convient de prendre des précautions lors de prescription de dorzolamide/timolol chez ces patients.
Un décollement de la choroïde a été rapporté lors d'administration de traitements diminuant la sécrétion de l'humeur aqueuse (par exemple timolol, acétazolamide) après chirurgie filtrante.
Comme avec d'autres antiglaucomateux, on a observé chez certains patients une diminution de la réponse au maléate de timolol ophtalmique lors de traitement prolongé. Cependant, dans des études cliniques au cours desquelles 164 patients ont été suivis pendant au moins trois ans, on n'a observé aucune différence significative de la pression intraoculaire moyenne après la stabilisation initiale.
Les patients avec antécédents d'allergie de contact à l'argent ne doivent pas utiliser ce médicament parce que les gouttes peuvent contenir des traces d'argent provenant du flacon.
Utilisation de lentilles de contact
Ce médicament n'a pas été étudié chez des patients porteurs de lentilles de contact.
Population pédiatrique
Voir rubrique 5.1
Condition de prescription
liste I
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Important
Présentation : 1 flacon(s) polyéthylène basse densité (PEBD) de 5 ml avec embout(s) polyéthylène haute densité (PEHD) siliconé(e)
Prix : 8.50
Taux de remboursement : 65%
Titulaire : SANTEN OY