VALGANCICLOVIR ARROW 450 mg, comprimé pelliculé
Classe médicamenteuse
antiviraux pour usage systémique, nucléosides et nucléotides autres que des inhibiteurs de transcriptase inverse | code ATC : J05AB14
Composition
Valganciclovir (sous forme de chlorhydrate de valganciclovir)................................................ 450 mg
Pour un comprimé pelliculé.
Excipient à effet notoire : aucun
Indications thérapeutiques
VALGANCICLOVIR ARROW est indiqué dans le traitement d’attaque et le traitement d’entretien de la rétinite à cytomégalovirus (CMV) chez les patients adultes atteints de syndrome d’immunodéficience acquise (SIDA).
VALGANCICLOVIR ARROW est indiqué en traitement prophylactique des infections à CMV chez les patients adultes et les enfants (dès la naissance jusqu’à 18 ans) CMV-négatifs ayant bénéficié d'une transplantation d’organe solide à partir d’un donneur CMV-positif.
Posologie et mode d'administration
Attention - Il est essentiel d'observer strictement les recommandations posologiques afin d'éviter un surdosage (voir rubriques 4.4 et 4.9).
Le valganciclovir est rapidement et largement métabolisé en ganciclovir après administration orale. Un traitement par le valganciclovir per os à 900 mg deux fois par jour équivaut à un traitement par le ganciclovir administré par voie IV à 5 mg/kg deux fois par jour.
Traitement de la rétinite à cytomégalovirus (CMV)
Patients Adultes
Traitement d’attaque de la rétinite à CMV :
Pour les patients présentant une rétinite à CMV active, la posologie recommandée est de 900 mg de valganciclovir (deux comprimés de VALGANCICLOVIR ARROW dosés à 450 mg) deux fois par jour pendant 21 jours ; les comprimés doivent être pris avec des aliments, dans la mesure du possible. Un traitement d’attaque prolongé peut accroître le risque de toxicité médullaire (voir rubrique 4.4).
Traitement d’entretien de la rétinite à CMV :
À la suite d’un traitement d’attaque ou chez les patients présentant une rétinite à CMV non évolutive, la posologie recommandée est de 900 mg de valganciclovir (deux comprimés de VALGANCICLOVIR ARROW dosés à 450 mg) une fois par jour ; les comprimés doivent être pris dans la mesure du possible avec des aliments. Le traitement d’attaque peut être répété chez les patients dont la rétinite s’aggrave. Cependant, la possibilité d’une résistance virale au médicament devra être envisagée.
La durée du traitement d’entretien doit être déterminée au cas par cas.
Population pédiatrique
La tolérance et l’efficacité de valganciclovir dans le traitement de la rétinite à CMV n’ont pas été établies au cours d’études cliniques adéquates et bien contrôlées menées chez des patients pédiatriques.
Traitement prophylactique de la maladie à CMV dans la transplantation d'organes solides
Chez les patients ayant reçu une greffe de rein, la posologie recommandée est de 900 mg (deux comprimés de Valganciclovir Arrow dosés à 450 mg) une fois par jour, le traitement doit être initié dans les 10 jours suivant la transplantation et poursuivi jusqu'à 100 jours après celle-ci. La prophylaxie peut être poursuivie jusqu’à 200 jours après la transplantation (voir rubriques 4.4, 4.8 et 5.1).
Chez les patients transplantés d’un organe solide autre que le rein, la posologie recommandée est de 900 mg (deux comprimés de Valganciclovir Arrow dosés à 450 mg) une fois par jour, le traitement devant être initié dans les 10 jours suivant la transplantation et poursuivi jusqu'à 100 jours après celle-ci.
Lorsque cela est possible, les comprimés doivent être administrés pendant un repas.
Chez les patients pédiatriques ayant reçu dès la naissance une greffe d’organe solide, qui présentent un risque de développer une maladie à CMV, la dose quotidienne unique recommandée de valganciclovir est calculée en fonction de la surface corporelle (SC) et de la clairance de la créatinine (ClCr), calculée à partir de la formule de Schwartz (ClCrS), selon l’équation suivante :
Posologie pédiatrique (mg) = 7 x SC x ClCrS (voir la formule de la surface corporelle de Mosteller et la formule de la clairance de la créatinine de Schwartz ci-dessous).
Si la clairance de la créatinine calculée selon la formule de Schwartz dépasse 150 ml/min/1,73 m², alors une valeur maximale de 150 ml/min/1,73 m² doit être utilisée dans l’équation :
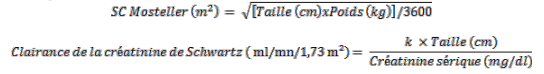
Où k = 0,45* pour les patients < 2 ans ; 0,55 pour les garçons de 2 à < 13 ans et pour les filles de 2 à 16 ans ; et 0,7 pour les garçons de 13 à 16 ans. Pour les patients de plus de 16 ans, se référer à la posologie de l’adulte.
Les valeurs de k sont basées sur la méthode de Jaffé pour la mesure de la créatinine sérique et peuvent nécessiter une correction lorsque des méthodes enzymatiques sont utilisées.
*Pour certaines sous-populations, une diminution de la valeur de k peut également être nécessaire (p.ex., chez les patients pédiatriques présentant un faible poids à la naissance).
Pour les patients pédiatriques ayant reçu une greffe de rein, la dose quotidienne unique recommandée en mg (7 x SC x ClCrS) doit être administrée dans les 10 jours suivant la transplantation et se poursuivre jusqu’à 200 jours après celle-ci.
Pour les patients pédiatriques ayant reçu une greffe d’organe solide autre que le rein, la dose quotidienne unique recommandée en mg (7 x SC x ClCrS) doit être administrée dans les 10 jours suivant la transplantation et se poursuivre jusqu’à 100 jours après celle-ci.
Toutes les doses calculées doivent être arrondies à l’incrément de 25 mg le plus proche pour la dose réelle administrable. Si la dose calculée dépasse 900 mg, il faut administrer une dose maximale de 900 mg. La solution buvable est la formulation recommandée dans la mesure où elle permet d’administrer une dose calculée selon la formule ci-dessus. Cependant, les comprimés pelliculés de valganciclovir peuvent être utilisés si la dose calculée est comprise dans un intervalle de 10 % des dosages disponibles en comprimés, et si le patient est en mesure d’avaler des comprimés. Par exemple, si la dose calculée est comprise entre 405 mg et 495 mg, un comprimé à 450 mg peut être administré.
Il est recommandé de contrôler les taux de créatinine sérique régulièrement et de prendre en compte les variations de taille et de poids corporel, puis d’adapter la posologie en conséquence au cours de la période de prophylaxie.
Instructions posologiques particulières
La posologie administrée aux patients pédiatriques ayant reçu une greffe d’organe solide est déterminée à partir de la fonction rénale du patient, et de sa surface corporelle.
Patients âgés :
La sécurité et l’efficacité n’ont pas été établies dans cette population. Aucune étude n’a été menée chez les patients âgés de plus de 65 ans. Étant donné que la fonction rénale diminue avec l’âge, le valganciclovir doit être administré aux patients âgés avec une attention particulière sur l’état de leur fonction rénale (voir le tableau ci-dessous) (voir rubrique 5.2).
Insuffisants rénaux :
La créatinine sérique ou la clairance de la créatinine estimée doivent être étroitement surveillées. La posologie doit être ajustée en fonction de la clairance de créatinine comme indiqué dans le tableau ci-dessous (voir rubriques 4.4 et 5.2).
La clairance de la créatinine (ml/min) peut être estimée à partir de la valeur de créatinine sérique au moyen des formules suivantes :
(140 - âge [ans]) x (poids corporel [kg])
Chez l’homme = -----------------------------------------------------------
(72) x (0,011 x créatinine sérique [micromoles/l])
Chez la femme = 0,85 x valeur chez l’homme.
|
ClCr (ml/min) |
Posologie du valganciclovir Traitement d'attaque |
Posologie du valganciclovir Traitement d'entretien - Prophylaxie |
|
≥ 60 |
900 mg (2 comprimés) 2 fois par jour |
900 mg (2 comprimés) 1 fois par jour |
|
40 - 59 |
450 mg (1 comprimé) 2 fois par jour |
450 mg (1 comprimé) 1 fois par jour |
|
25 - 39 |
450 mg (1 comprimé) 1 fois par jour |
450 mg (1 comprimé) tous les 2 jours |
|
10 - 24 |
450 mg (1 comprimé) tous les 2 jours |
450 mg (1 comprimé) 2 fois par semaine |
|
< 10 |
Non recommandé |
Non recommandé |
Patients hémodialysés :
Pour les patients sous hémodialyse (ClCr < 10 ml/min), il n’est pas possible de recommander une posologie. Par conséquent, le valganciclovir comprimé pelliculé ne doit pas être utilisé chez ces patients (voir rubriques 4.4 et 5.2).
Insuffisants hépatiques :
La sécurité et l’efficacité de comprimés de valganciclovir n’ont pas été établies chez l’insuffisant hépatique (voir rubrique 5.2).
Patients présentant une leucopénie, neutropénie, anémie, thrombopénie ou pancytopénie sévère :
Voir rubrique 4.4 avant de débuter le traitement.
En cas de dégradation significative de la numération formule sanguine au cours du traitement par le valganciclovir, l’administration de facteurs de croissance hématopoïétique et/ou l’interruption du traitement doivent être envisagées (voir rubrique 4.4).
Mode d’administration
Le valganciclovir est administré par voie orale et doit, dans la mesure du possible, être pris avec des aliments (voir rubrique 5.2).
Pour les patients pédiatriques qui ne sont pas en mesure d’avaler les comprimés pelliculés, une autre forme pharmaceutique peut être utilisée, par exemple, la poudre pour solution buvable.
Précautions à prendre avant de manipuler ou d’administrer le médicament
Les comprimés ne doivent être ni cassés ni broyés. Le valganciclovir étant considéré comme potentiellement tératogène et carcinogène chez l’homme, des précautions doivent être prises pour la manipulation des comprimés cassés (voir rubrique 4.4). Éviter le contact direct des comprimés cassés ou broyés avec la peau ou les muqueuses. En cas de contact, laver abondamment au savon et à l’eau ; rincer abondamment les yeux à l’eau stérile ou à l’eau courante en l’absence d’eau stérile.
Voie d'administration
orale
Contre-indications
Hypersensibilité au valganciclovir, ganciclovir ou à l’un des excipients mentionnés à la rubrique 6.1.
VALGANCICLOVIR ARROW est contre-indiqué durant l’allaitement (voir rubrique 4.6).
Mise en garde et précautions d'emploi
Hypersensibilité croisée
En raison de la similarité de la structure chimique du ganciclovir et de celle de l’aciclovir et du penciclovir, une réaction d’hypersensibilité croisée entre ces médicaments est possible. VALGANCICLOVIR ARROW doit donc être prescrit avec prudence chez les patients présentant une hypersensibilité connue à l’aciclovir ou au penciclovir (ou à leurs prodrogues respectives le valaciclovir ou le famciclovir).
Mutagénicité, tératogénicité, carcinogénicité, fertilité et contraception
Avant l’initiation du traitement par le valganciclovir, les patients doivent être avertis des risques potentiels pour le fœtus. Les études chez l’animal ont montré que le ganciclovir est mutagène, tératogène, aspermatogénique et carcinogène et altère la fertilité chez les femelles. Le valganciclovir doit donc être considéré comme potentiellement tératogène et carcinogène chez l’homme, et peut causer des malformations congénitales et des cancers (voir rubrique 5.3). D’après des études cliniques et non cliniques, il est également probable que le valganciclovir provoque une inhibition temporaire ou définitive de la spermatogenèse. Les femmes en âge de procréer doivent être informées de la nécessité d’utiliser une méthode de contraception efficace durant le traitement et pendant au moins 30 jours après le traitement. Les hommes doivent être informés de la nécessité d’avoir recours à une méthode de contraception mécanique durant le traitement, et pendant au moins 90 jours après le traitement, sauf s’il est certain que la partenaire n'est pas à risque de procréer (voir rubriques 4.6, 4.8 et 5.3).
Le valganciclovir est potentiellement carcinogène et toxique à long terme sur la reproduction.
Myélosuppression
Une leucopénie, une neutropénie, une anémie, une thrombopénie, une pancytopénie, une insuffisance médullaire et une anémie d'origine centrale, toutes de caractère sévère, ont été observées chez des patients traités par valganciclovir (et ganciclovir). Aucun traitement ne doit être initié si le nombre absolu des polynucléaires neutrophiles est inférieur à 500 cellules/µl, ou le nombre des plaquettes est inférieur à 25 000/µl, ou le taux d’hémoglobine est inférieur à 8 g/dl (voir rubriques 4.2 et 4.8).
Lorsque la prophylaxie est prolongée au-delà de 100 jours, le risque éventuel de développer une leucopénie et une neutropénie doit être pris en compte (voir sections 4.2, 4.8 et 5.1).
Le valganciclovir doit être utilisé avec précaution chez les patients ayant une cytopénie hématologique préexistante ou des antécédents de cytopénie hématologique d’origine médicamenteuse, ainsi que chez les patients sous radiothérapie.
Il est recommandé de surveiller régulièrement la numération formule sanguine et le nombre des plaquettes durant le traitement. Une surveillance hématologique plus étroite peut être nécessaire chez les insuffisants rénaux et chez les enfants, au minimum à chaque fois que le patient se rend à un rendez-vous dans l’établissement dans lequel il a été greffé. Chez les patients développant une leucopénie, une neutropénie, une anémie et/ou une thrombopénie de caractère sévère, il est recommandé d’envisager un traitement par facteurs de croissance hématopoïétique et/ou une interruption du traitement (voir rubrique 4.2).
Différence de biodisponibilité avec ganciclovir par voie orale
La biodisponibilité du ganciclovir après administration unique de 900 mg de valganciclovir est d’environ 60 % comparée à environ 6 % après administration orale de 1 000 mg de ganciclovir (en gélules). Une exposition excessive au ganciclovir peut entraîner des effets indésirables pouvant menacer le pronostic vital. Il est donc conseillé de respecter scrupuleusement les posologies recommandées lors de l’instauration du traitement, lors du passage du traitement d’attaque au traitement d’entretien, ainsi que chez les patients qui passent du ganciclovir oral au valganciclovir, étant donné que ce dernier ne peut être substitué au ganciclovir en gélules sur la base d’un comprimé pour une gélule. Les patients passant des gélules de ganciclovir au valganciclovir doivent être avertis du risque de surdosage s’ils prennent un nombre de comprimés de valganciclovir supérieur au nombre prescrit (voir rubriques 4.2 et 4.9).
Insuffisance rénale
Chez les insuffisants rénaux, la posologie doit être ajustée en fonction de la clairance de la créatinine (voir rubriques 4.2 et 5.2).
Le valganciclovir en comprimé pelliculé ne doit pas être utilisé chez les patients sous hémodialyse (voir rubriques 4.2 et 5.2).
Utilisation avec d’autres médicaments
Des convulsions ont été rapportées chez des patients recevant de l’imipénème-cilastatine et du ganciclovir. Le valganciclovir ne doit pas être utilisé en même temps que l’imipénème-cilastatine, sauf si les bénéfices attendus justifient les risques encourus (voir rubrique 4.5).
Chez les patients traités par le valganciclovir et par (a) la didanosine, (b) des médicaments connus comme myélosuppresseurs (par exemple, la zidovudine), ou (c) des substances modifiant la fonction rénale, la recherche de signes de toxicité accrue devra être étroitement surveillée (voir rubrique 4.5).
L’essai clinique contrôlé utilisant le valganciclovir dans le traitement prophylactique de la maladie à CMV en cas de transplantation tel que décrit dans la rubrique 5.1 ne comprenait pas de patients ayant bénéficié d’une greffe de poumon ou d’intestin. Par conséquent, l’expérience chez ces patients transplantés reste limitée.
Condition de prescription
liste I
Groupe générique
VALGANCICLOVIR (CHLORHYDRATE DE) équivalant à valganciclovir 450 mg - ROVALCYTE 450 mg, comprimé pelliculé
Liste des médicaments de ce groupe de générique.Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Non disponible
Présentation : plaquette(s) polyamide aluminium PVC-Aluminium de 60 comprimé(s)
Prix : 591.13
Taux de remboursement : 65%
Titulaire : ARROW GENERIQUES