CARBOPLATINE TEVA 10 mg/ml, solution pour perfusion
Classe médicamenteuse
autres antinéoplasiques | code ATC : L01XA02
Composition
Carboplatine ......................................................................................................................... 10 mg
Pour 1 mL.
Indications thérapeutiques
- Carcinome de l'ovaire d'origine épithéliale.
- Carcinome bronchique à petites cellules.
- Carcinome épidermoïde des voies aérodigestives supérieures.
Posologie et mode d'administration
Posologie
Monochimiothérapie
La posologie recommandée de carboplatine chez les malades non pré-traités antérieurement par une chimiothérapie cytotoxique et dont la fonction rénale est normale est de 400 mg/m2, injectés par perfusion intraveineuse de 15 à 60 min. Le traitement ne devrait pas être répété avant un délai de 4 semaines, après l'administration précédente du carboplatine et/ou tant que le nombre de neutrophiles n'est pas supérieur ou égal à 2 000/mm3 et le nombre de plaquettes à 100 000/mm3.
Une diminution de 20 à 25 % de cette posologie initiale est recommandée chez les malades présentant des facteurs de risque tels qu'une chimiothérapie antérieure ou un mauvais état général (ECOG-Zubrod 2-4 ou Karnofsky inférieur à 80).
Les modifications éventuelles de posologie lors des cures suivantes seront déterminées par la surveillance hebdomadaire des paramètres hématologiques (nadir hématologique).
Traitement en association
L’utilisation optimale du carboplatine avec d’autres agents myélosuppresseurs nécessite des ajustements posologiques en fonction du protocole thérapeutique et du calendrier adoptés.
Insuffisance rénale
Les patients ayant une clairance de la créatinine inférieure à 60 mL/min sont exposés à un risque plus élevé de myélosuppression sévère. La fréquence des leucopénies, neutropénies ou thrombocytopénies sévères a pu être maintenue à environ 25% en suivant les recommandations posologiques ci-dessous :
|
Clairance initiale de la créatinine |
Dose initiale (jour 1) |
|
41-59 mL/min. |
250 mg/m2 |
|
16-40 mL/min. |
200 mg/m2 |
Les données concernant l'utilisation du carboplatine injectable chez les patients dont la clairance de la créatinine est ≤ 15 mL/min sont insuffisantes pour établir une recommandation de traitement.
Toutes les recommandations posologiques mentionnées ci-dessus s'appliquent à la première cure de traitement. Les posologies suivantes devront être ajustées en fonction de la tolérance du patient au traitement et du degré acceptable de myélosuppression.
Autres méthodes de détermination de posologie (en mono ou polychimiothérapie, y compris dans le cas d'insuffisance rénale)
L'adaptation individuelle des posologies de carboplatine peut aussi être approchée en utilisant la formule de Calvert ou la formule d'Egorin.
- La formule de Calvert tient compte du débit de filtration glomérulaire (GFR en mL/min.) et de l'aire sous la courbe (AUC en mg/mL x min.) :
Dose (mg) = AUC x (GFR + 25) (la formule de Calvert calcule la dose totale en mg, et non en mg/m2).
La méthode de référence pour déterminer le débit de filtration glomérulaire (GFR) est la mesure de la clairance à l'EDTA marqué au chrome 51 qui implique la manipulation de produits radioactifs. En pratique, on estime que le débit est correctement évalué par la clairance de la créatinine (Clcr), elle-même estimée grâce à la méthode prédictive de Jeliffe qui tient compte de l'âge, du sexe et de la créatininémie plasmatique (Pcr) :
GFR (femme) = 0,9 x GFR (homme)
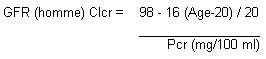
Les AUC cibles sont fonction des éventuels traitements antérieurs et du protocole thérapeutique selon que le carboplatine est utilisé seul ou en association :
|
AUC cible |
Chimiothérapie envisagée |
Traitement antérieur |
|
6 - 8 mg/mL x min. |
Carboplatine en monothérapie |
Patient non pré-traité |
|
4 - 6 mg/mL x min. |
Carboplatine en monothérapie |
Patient pré-traité |
|
4 - 6 mg/mL x min. |
Carboplatine en association |
Patient non pré-traité |
Remarque : les valeurs d'AUC ont été validées pour le carboplatine en association avec le cyclophosphamide chez les patients non pré-traités et avec l'étoposide chez les patients pré-traités et non pré-traités.
- La formule d'Egorin calcule la dose totale en mg/m2 :
Patient non pré-traité par chimiothérapie :

Patient pré-traité par chimiothérapie :

Patients âgés
Chez les patients de plus de 65 ans, un ajustement posologique du carboplatine est nécessaire au cours de la première cure et lors des cures suivantes.
Population pédiatrique
Dans l'état actuel des connaissances, il n'est pas possible de recommander une posologie particulière pour l'utilisation pédiatrique du carboplatine.
Mode d’administration
Voie d'administration : perfusion intraveineuse exclusivement.
Les différents dosages de carboplatine peuvent être administrés tels quels à la concentration de 10 mg/mL en dérivation d'une perfusion de solution de glucose à 5 %. Ils peuvent aussi être dilués avant administration à l'aide d'une solution de glucose à 5%, jusqu'à une concentration minimale de 0,5 mg/mL. Dans tous les cas, il est recommandé après perfusion de carboplatine de rincer la veine avec une solution de glucose à 5 %.
Modalités de manipulation
La préparation des solutions injectables de cytotoxiques doit être obligatoirement réalisée par un personnel spécialisé et entraîné ayant une connaissance des médicaments utilisés, dans des conditions assurant la protection de l'environnement et surtout la protection du personnel qui manipule. Elle nécessite un local de préparation réservé à cet usage. Il est interdit de fumer, de manger, de boire dans ce local. Les manipulateurs doivent disposer d'un ensemble de matériel approprié à la manipulation notamment de blouses à manches longues, masques de protection, calot, lunettes de protection, gants à usage unique stériles, champs de protection du plan de travail, conteneurs et sacs de collecte des déchets. Les excreta et les vomissures doivent être manipulés avec précaution. Les femmes enceintes doivent être averties et éviter la manipulation de cytotoxiques. Tout contenant cassé doit être traité avec les mêmes précautions et considéré comme un déchet contaminé. L'élimination des déchets contaminés se fait par incinération dans des conteneurs rigides étiquetés à cet effet.
Ces dispositions peuvent être envisagées dans le cadre du réseau de cancérologie (circulaire DGS/DH/98 N° 98/188 du 24 mars 1998) en collaboration avec toute structure adaptée et remplissant les conditions requises.
Remarque :
Aucun des composants nécessaires à l'administration intraveineuse par perfusion du carboplatine (aiguilles ou les kits d’administration IV) ne doit contenir en totalité ou en partie de l'aluminium. En effet, une interaction entre l'aluminium et le carboplatine peut être à l’origine d'un précipité et/ou d’une perte d’efficacité.
Voie d'administration
intraveineuse
Contre-indications
- Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
- Insuffisance rénale sévère (clairance de la créatinine < 30 ml/min, sauf si le médecin et le patient, jugent que les bénéfices possibles du traitement soient supérieurs aux risques).
- Myélosuppression sévère.
- Tumeurs hémorragiques.
- En association avec le vaccin contre la fièvre jaune (voir rubrique 4.5).
- Grossesse, sauf en cas d’absence d’alternative thérapeutique appropriée.
- Allaitement.
Mise en garde et précautions d'emploi
Les injections de carboplatine ne doivent être pratiquées que par des médecins expérimentés dans la chimiothérapie anticancéreuse. Des numérations sanguines ainsi que des explorations fonctionnelles hépatiques et rénales doivent être effectuées régulièrement; et le carboplatine doit être arrêté si une dépression médullaire anormale ou une anomalie de la fonction rénale ou hépatique survient.
Toxicité hématologique
Les leucopénies, neutropénies, et thrombocytopénies sont dose-dépendantes et dose-limitantes. Les paramètres hématologiques doivent être fréquemment contrôlés avant chaque cure et dans l'intervalle des cycles ; et en cas de toxicité, jusqu’à ce que le rétablissement soit atteint.
Le nadir moyen de la leucopénie se situe au 21e jour chez les patients recevant le carboplatine en injection, et au 15e jour chez les patients recevant une injection de carboplatine associée à d’autres agents de chimiothérapie. Celui de la thrombopénie se situe au 15e jour (entre le 14e et le 21e) après le traitement. En général, les cures uniques d’administrations intermittentes de carboplatine par injection ne doivent pas être répétées jusqu'à ce que les taux de leucocytes, de neutrophiles et de plaquettes soient revenus à la normale. Le traitement ne doit pas être répété moins de 4 semaines entre chaque administration de carboplatine et/ou jusqu'à ce que le nombre de neutrophiles soit d'au moins 2000 cellules/mm3 et que le nombre de plaquettes soit d'au moins 100 000 cellules /mm3.
L'anémie est fréquente et cumulative, et nécessite dans de très rares cas une transfusion.
L’anémie hémolytique, avec la présence d’anticorps induits par des médicaments sérologiques, a été rapportée chez des patients traités par carboplatine. Cet évènement peut être fatal.
La gravité de la myélosuppression est augmentée chez les patients ayant reçu au préalable un traitement (en particulier avec le cisplatine) et/ou présentant une anomalie de la fonction rénale. Chez ces patients, les doses initiales de carboplatine à injecter devraient être réduites de manière appropriée (voir rubrique 4.2); et les effets doivent être surveillés attentivement, par de fréquentes numérations sanguines entre les différentes cures. L’injection de carboplatine en association avec d'autres agents myélosuppresseurs doit être envisagée avec beaucoup de prudence en respectant les doses et les intervalles de temps, afin de minimiser les effets cumulatifs des molécules.
Les effets myélosuppresseurs peuvent s’ajouter à ceux de la chimiothérapie concomitante. Les patients souffrant d’une myélosuppression sévère et persistante sont à risque élevé de complications infectieuses, pouvant être d’issue fatale (voir rubrique 4.8). Si l’un de ces événements survient, le traitement par carboplatine doit être interrompu et une adaptation posologique ou un arrêt du traitement doivent être envisagés.
Des cas de leucémie promyélocytaire aiguë et de syndrome myélodysplasique (SMD)/leucémie myéloïde aiguë (LMA) ont été rapportés des années après le traitement par carboplatine et autres traitements antinéoplasiques.
Syndrome hémolytique et urémique (SHU)
Le syndrome hémolytique et urémique (SHU) est un effet indésirable menaçant le pronostic vital. Le carboplatine doit être interrompu dès les premiers signes d'une anémie hémolytique microangiopathique, comme une chute brutale de l'hémoglobine associée à une thrombopénie, une élévation de la bilirubine sérique, de la créatinine sérique, de l'urée sanguine, ou de la LDH. L'insuffisance rénale peut ne pas être réversible à l'arrêt du traitement et une dialyse peut s’avérer nécessaire.
Réactions d’hypersensibilité
Comme avec d'autres médicaments à base de platine, des réactions allergiques, apparaissant le plus souvent pendant la perfusion, peuvent se produire, et nécessiter l'arrêt de la perfusion, ainsi qu’un traitement symptomatique approprié. Des réactions croisées, parfois fatales, ont été rapportées avec tous les organoplatines (voir la section 4.3 et rubrique 4.8).
Des cas de réactions d’hypersensibilité ayant évolué vers un syndrome de Kounis (spasme coronarien allergique aigu pouvant entraîner un infarctus du myocarde, voir rubrique 4.8) ont été rapportés.
Toxicité rénale
Chez les patients dont la fonction rénale est altérée, l'effet du carboplatine sur le système hématopoïétique est plus prononcé, dure plus longtemps que chez les patients ayant une fonction rénale normale. Dans ce groupe à risque, le traitement par carboplatine doit être envisagé avec une précaution particulière (voir rubrique 4.2).
Neurotoxicité
Bien que la toxicité neurologique périphérique soit généralement fréquente et modérée, limitée à des paresthésies et à une diminution des réflexes ostéotendineux, sa fréquence est augmentée chez les patients de plus de 65 ans, et/ou ayant été traités au préalable par cisplatine. Une surveillance neurologique régulière est recommandée.
Des troubles visuels, et notamment une perte de la vision, ont été rapportés après utilisation de carboplatine en injection, à des doses supérieures à celles recommandées chez les patients atteints d'insuffisance rénale. La vision semble se rétablir totalement ou de façon significative dans les semaines suivant l'arrêt de ces doses élevées.
Population âgée
Dans les études où le carboplatine et le cyclophosphamide étaient administrés en association, les patients âgés traités par du carboplatine étaient plus susceptibles de développer une thrombocytopénie sévère que les patients plus jeunes. Parce que la fonction rénale est souvent diminuée chez le sujet âgé, celle-ci doit être évaluée pour déterminer la posologie (voir rubrique 4.2).
Syndrome de leucoencéphalopathie postérieure réversible (SLPR)
Des cas de syndrome de leucoencéphalopathie postérieure réversible (SLPR) ont été rapportés chez des patients recevant du carboplatine associé à une chimiothérapie. Le SLPR est une maladie neurologique rare, réversible à l'arrêt du traitement, d’évolution rapide, pouvant se manifester par des crises convulsives, une hypertension, des céphalées, de la confusion, une cécité et d'autres troubles visuels et neurologiques (voir rubrique 4.8). Le diagnostic de SLPR est confirmé par l’imagerie cérébrale, de préférence l'IRM (imagerie par résonance magnétique).
Maladie veino-occlusive hépatique
Des cas de maladie veino-occlusive hépatique (syndrome d’obstruction sinusoïdale) ont été rapportés, dont certains étaient mortels. Les patients doivent être surveillés pour des signes et des symptômes de fonction hépatique anormale ou d’hypertension portale ne résultant pas de manière évidente de métastases hépatiques.
Syndrome de lyse tumorale (SLT)
Dans l’expérience de post-mise sur le marché, le syndrome de lyse tumorale (SLT) a été rapporté chez les patients suite à l’utilisation de carboplatine seul ou en association avec d’autres agents chimiothérapeutiques. Les patients à risque élevé de SLT, comme les patients présentant un taux prolifératif élevé, une charge tumorale élevée et une haute sensibilité à des agents cytotoxiques, doivent être étroitement surveillés et des précautions appropriées doivent être prises.
Autres
Des déficits auditifs ont été rapportés au cours du traitement par carboplatine. L’ototoxicité peut être plus prononcée chez les enfants. Des cas de perte auditive d’apparition tardive ont été rapportés dans la population pédiatrique. Un suivi audiométrique à long terme est recommandé dans cette population.
L'administration de vaccins vivants ou vivants atténués à des patients immunodéprimés par des agents de chimiothérapie, dont le carboplatine, peut entraîner des infections graves ou mortelles. La vaccination avec un vaccin vivant doit être évitée chez les patients recevant le carboplatine. Les vaccins tués ou inactivés peuvent être administrés mais la réponse à ces vaccins peut être plus faible.
Condition de prescription
médicament nécessitant une surveillance particulière pendant le traitement
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Non disponible
Présentation : 1 flacon(s) en verre brun de 5 ml
Prix : non disponible
Taux de remboursement : 0%
Titulaire : TEVA SANTE