SPIRIVA RESPIMAT 2,5 microgrammes/dose, solution à inhaler
Classe médicamenteuse
Autres médicaments pour les syndromes obstructifs des voies aériennes par inhalation, anticholinergiques | code ATC : R03B
Composition
Tiotropium…………………………………………………………………….………………2,5 microgrammes
Sous forme de bromure de tiotropium monohydraté…………………………….…...3,124 microgrammes
pour une bouffée délivrée à la sortie de l’embout buccal
La dose délivrée par bouffée correspond à la quantité de tiotropium délivré à la sortie de l’embout buccal.
La dose journalière correspond à 2 bouffées.
Excipient à effet notoire : ce médicament contient 0,0011 mg de chlorure de benzalkonium par bouffée.
Indications thérapeutiques
Bronchopneumopathie chronique obstructive (BPCO)
SPIRIVA RESPIMAT est indiqué en traitement bronchodilatateur continu destiné à soulager les symptômes des patients présentant une bronchopneumopathie chronique obstructive.
Asthme
SPIRIVA RESPIMAT est indiqué en traitement bronchodilatateur additionnel continu chez des patients de 6 ans et plus atteints d’asthme sévère qui ont présenté au cours de l’année précédente une ou plusieurs exacerbations sévères d’asthme (voir rubriques 4.2 et 5.1).
Posologie et mode d'administration
Posologie
Voie inhalée exclusivement.
La cartouche ne peut être insérée et utilisée qu’avec l’inhalateur RESPIMAT.
La dose journalière est de 2 bouffées successives (soit 2 pressions sur le bouton) administrées à l’aide de l’inhalateur RESPIMAT.
La posologie recommandée chez l’adulte est de 5 microgrammes de tiotropium, soit 2 bouffées successives (soit 2 pressions sur le bouton) administrées à l’aide de l’inhalateur RESPIMAT, en une prise par jour, à heure fixe dans la journée.
Ne pas dépasser la dose recommandée.
Dans le traitement de l’asthme, le bénéfice complet peut n’apparaître qu’après plusieurs jours de traitement. Chez les patients adultes atteints d’asthme sévère, le tiotropium doit être utilisé en association à un corticostéroïde inhalé (CSI) (≥ 800 µg de budésonide/jour ou équivalent) et au moins un traitement de contrôle.
Populations particulières
Sujets âgés : le bromure de tiotropium peut être utilisé chez les sujets âgés sans adaptation de la posologie.
Insuffisance rénale : en cas d’insuffisance rénale, le bromure de tiotropium peut être utilisé sans adaptation de la posologie. En cas d’insuffisance rénale modérée à sévère (clairance de la créatinine £ 50 ml/min) voir rubriques 4.4 et 5.2.
Insuffisance hépatique : en cas d’insuffisance hépatique, le bromure de tiotropium peut être utilisé sans adaptation de la posologie (voir rubrique 5.2).
Population pédiatrique
Asthme : la posologie recommandée chez les patients âgés de 6 à 17 ans est de 5 microgrammes de tiotropium, soit 2 bouffées consécutives administrées à l’aide de l’inhalateur RESPIMAT, en une prise par jour, à heure fixe dans la journée.
Chez les adolescents (12-17 ans) atteints d’asthme sévère, le tiotropium doit être utilisé en association à un CSI (> 800-1600 µg de budésonide/jour ou équivalent) et un traitement de contrôle ou en association à un CSI (400-800 µg de budésonide/jour ou équivalent) et deux traitements de contrôle.
Chez les enfants (6-11 ans) atteints d’asthme sévère, le tiotropium doit être utilisé en association à un CSI (> 400 µg de budésonide/jour ou équivalent) et un traitement de contrôle ou en association à un CSI (200‑400 µg de budésonide/jour ou équivalent) et deux traitements de contrôle.
La sécurité et l’efficacité de SPIRIVA RESPIMAT chez les enfants âgés de 6 à 17 ans atteints d’asthme modéré n’ont pas encore été établies. La sécurité et l’efficacité de SPIRIVA RESPIMAT chez les enfants de moins de 6 ans n’ont pas été établies. Les données actuellement disponibles sont décrites dans les rubriques 5.1 et 5.2 mais aucune recommandation sur la posologie ne peut être faite.
BPCO : il n’y a pas de justification à l’utilisation de SPIRIVA RESPIMAT chez les enfants et les adolescents de moins de 18 ans.
Mucoviscidose : la sécurité et l’efficacité de SPIRIVA RESPIMAT n’ont pas été établies (voir rubriques 4.4 et 5.1).
Mode d’administration
Ce médicament est destiné à l’inhalation uniquement. La cartouche ne peut être insérée et utilisée qu’avec l’inhalateur RESPIMAT réutilisable. Le dispositif RESPIMAT est un inhalateur qui génère une pulvérisation pour inhalation. Ce dispositif est destiné à un seul patient et pour l’administration de plusieurs doses délivrées par une cartouche. L’inhalateur RESPIMAT réutilisable permet le remplacement des cartouches et peut être utilisé avec jusqu’à 6 cartouches.
Les patients doivent lire les instructions d’utilisation de l’inhalateur RESPIMAT réutilisable avant de commencer à utiliser SPIRIVA RESPIMAT.
Pour une administration correcte du médicament, le médecin ou un autre professionnel de santé devra s’assurer du bon usage de l’appareil par le patient.
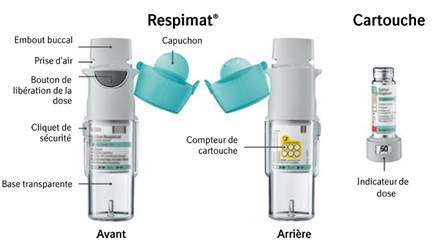
Mode d’emploi pour la manipulation et l’utilisation de l’inhalateur RESPIMAT réutilisable
Les enfants doivent utiliser SPIRIVA RESPIMAT avec l’aide d’un adulte.
Le patient utilisera cet inhalateur UNE SEULE FOIS PAR JOUR. A chaque utilisation, prendre 2 BOUFFEES (soit 2 pressions sur le bouton de libération de la dose).
- Si SPIRIVA RESPIMAT n’a pas été utilisé pendant plus de 7 jours, exercer une pression sur le bouton pour libérer une bouffée vers le sol.
- Si SPIRIVA RESPIMAT n’a pas été utilisé pendant plus de 21 jours, répéter les étapes 4 à 6 « Préparation pour l’utilisation » ci-dessous jusqu'à ce qu'un nuage apparaisse. Puis, répéter les étapes 4 à 6 trois fois supplémentaires.
Comment entretenir l'inhalateur RESPIMAT réutilisable
Nettoyer l’embout buccal, y compris la partie métallique à l’intérieur de l’embout buccal, en utilisant uniquement un linge ou un tissu humide, au moins une fois par semaine.
L’apparition d’une décoloration mineure de l’embout buccal n’affecte pas les performances de l'inhalateur RESPIMAT réutilisable.
Si nécessaire, essuyer l’extérieur de l'inhalateur RESPIMAT réutilisable avec un linge humide.
Quand se procurer un nouvel inhalateur
Une fois que le patient a utilisé l’inhalateur avec 6 cartouches, il doit se procurer une nouvelle boîte de SPIRIVA RESPIMAT contenant un inhalateur.


Préparation pour l’utilisation
|
1. Retirer la base transparente - Maintenir le capuchon fermé. - Appuyer sur le cliquet de sécurité tout en retirant la base transparente avec l'autre main.
|
|
|
2. Insérer la cartouche - Insérer la cartouche dans l’inhalateur. - Placer l’inhalateur sur une surface solide et pousser fermement jusqu’à ce qu’il se mette en place. |
|
|
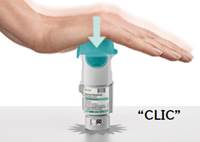
3. Surveiller le nombre de cartouches utilisées et remettre la base transparente - Cocher la case sur l’étiquette de l’inhalateur pour comptabiliser le nombre de cartouches utilisées. - Remettre en place la base transparente jusqu’à entendre un déclic.
|
|
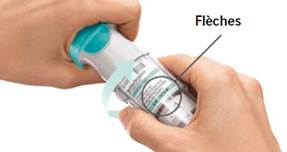
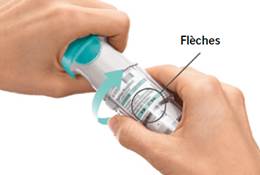
4. Tourner - Maintenir le capuchon fermé. - Tourner la base transparente dans la direction des flèches imprimées sur l’étiquette jusqu’à entendre un déclic (un demi-tour).
|
|
|
5. Ouvrir - Ouvrir complètement le capuchon. |
|
|
6. Presser - Diriger l’inhalateur en direction du sol. - Presser le bouton de libération de la dose. - Fermer le capuchon. - Répéter les étapes 4 à 6 jusqu’à ce qu’un nuage apparaisse. - A l’apparition du nuage, répéter les étapes 4 à 6 trois fois supplémentaires. L’inhalateur est maintenant prêt à être utilisé et 60 bouffées pourront être libérées (soit 30 doses). |
|
Utilisation quotidienne
|
TOURNER - Maintenir le capuchon fermé. - TOURNER la base transparente dans la direction des flèches imprimées sur l’étiquette jusqu’à entendre un déclic (un demi-tour).
|
|
|
OUVRIR OUVRIR complétement le capuchon |
|
|
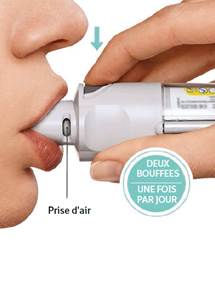
PRESSER - Expirer lentement et complètement en dehors du dispositif. - Fermer les lèvres autour de l’embout buccal sans recouvrir les prises d’air. Diriger l'embout buccal de l’inhalateur vers le fond de la gorge. - Tout en inspirant lentement et profondément par la bouche, PRESSER le bouton de libération de la dose et continuer d’inspirer lentement aussi longtemps que possible sans être gêné. - Bloquer la respiration pendant 10 secondes ou aussi longtemps que possible sans être gêné. - Répéter TOURNER, OUVRIR, PRESSER sur le bouton pour délivrer la 2ème bouffée (2 bouffées successives au total). - Fermer le capuchon jusqu’à la prochaine utilisation de l'inhalateur.
|
|
Quand remplacer la cartouche de SPIRIVA RESPIMAT
L’indicateur de dose indique le nombre de bouffées restantes dans la cartouche.
![]()
60 bouffées (60 pressions) restantes.
![]()
Moins de 10 bouffées (10 pressions) restantes. Se procurer une nouvelle cartouche.
![]() La cartouche est vide. Tourner la base transparente afin de la retirer. L’inhalateur est maintenant en position verrouillée. Retirer la cartouche de l’inhalateur. Insérer une nouvelle cartouche jusqu’à entendre un déclic (se référer à l’étape 2). La nouvelle cartouche dépassera davantage que la toute première cartouche (continuer avec l'étape 3). Ne pas oublier de remettre la base transparente pour déverrouiller l'inhalateur.
La cartouche est vide. Tourner la base transparente afin de la retirer. L’inhalateur est maintenant en position verrouillée. Retirer la cartouche de l’inhalateur. Insérer une nouvelle cartouche jusqu’à entendre un déclic (se référer à l’étape 2). La nouvelle cartouche dépassera davantage que la toute première cartouche (continuer avec l'étape 3). Ne pas oublier de remettre la base transparente pour déverrouiller l'inhalateur.
Voie d'administration
inhalée
Contre-indications
Hypersensibilité (allergie) au bromure de tiotropium, à l'un des excipients mentionnés à la rubrique 6.1, ou à l'atropine ou ses dérivés, par exemple l'ipratropium ou l'oxitropium.
Mise en garde et précautions d'emploi
Excipients
Le chlorure de benzalkonium contenu dans ce médicament peut provoquer une respiration sifflante et des difficultés respiratoires. Les patients asthmatiques ont un risque élevé de présenter ces événements indésirables.
Le bromure de tiotropium est un traitement bronchodilatateur continu de longue durée d’action en une prise par jour. Il ne doit pas être utilisé comme un médicament de première intention pour le traitement des épisodes aigus de bronchospasme ou pour le soulagement des symptômes aigus. En cas de crise d’asthme, un bêta-2-agoniste d’action rapide doit être utilisé.
SPIRIVA RESPIMAT ne doit pas être utilisé en monothérapie dans le traitement de l’asthme. Lors de la mise en route du traitement par SPIRIVA RESPIMAT, les patients asthmatiques doivent être informés qu’ils doivent continuer leur traitement anti-inflammatoire par corticostéroïdes inhalés sans le modifier même si les symptômes s’améliorent.
Des réactions d’hypersensibilité immédiate peuvent survenir après l’inhalation du bromure de tiotropium.
En raison de son activité anticholinergique, le bromure de tiotropium doit être utilisé avec prudence en cas de glaucome à angle fermé, d'hypertrophie de la prostate ou de rétrécissement du col de la vessie.
D’une façon générale, l’administration par voie inhalée des médicaments peut déclencher un bronchospasme.
Le tiotropium doit être utilisé avec prudence chez les patients ayant eu un infarctus du myocarde au cours des six derniers mois, une arythmie cardiaque instable ou menaçant le pronostic vital, une arythmie cardiaque ayant nécessité une intervention ou une modification du traitement médicamenteux au cours de l’année précédente, ou chez les patients ayant été hospitalisés pour une insuffisance cardiaque (NYHA classe III ou IV) au cours de l’année précédente. Les patients ayant de tels antécédents ont été exclus des essais cliniques et un retentissement lié à l'activité anticholinergique du tiotropium dans ces situations n'est pas exclu.
Les concentrations plasmatiques de bromure de tiotropium augmentent chez les patients présentant une fonction rénale altérée. Par conséquent, en cas d'insuffisance rénale modérée à sévère (clairance de la créatinine £ 50 ml/min), le bromure de tiotropium ne doit être utilisé que si le bénéfice attendu est supérieur au risque potentiel. A ce jour, il n'y a pas d'expérience à long terme avec le tiotropium chez les patients présentant une insuffisance rénale sévère (voir rubrique 5.2).
Il conviendra d’avertir les patients du risque de déclenchement ou d’aggravation d'un glaucome à angle fermé, de douleur ou gêne oculaire, de vision trouble transitoire avec halo visuel ou images colorées associée à une rougeur oculaire et un œdème cornéo-conjonctival, en cas de projection intraoculaire du produit. Si un ou plusieurs de ces symptômes oculaires apparaissent, les patients doivent interrompre l’utilisation du bromure de tiotropium et consulter immédiatement un médecin.
La sécheresse buccale observée avec les traitements anticholinergiques en général, peut à long terme favoriser la survenue de caries dentaires.
La posologie du bromure de tiotropium ne doit pas dépasser une prise par jour (voir rubrique 4.9).
SPIRIVA RESPIMAT n’est pas recommandé dans le traitement de la mucoviscidose. En cas d’utilisation chez des patients atteints de mucoviscidose, SPIRIVA RESPIMAT peut augmenter les signes et symptômes de la mucoviscidose (par exemple : événements indésirables graves, exacerbations pulmonaires, infections des voies respiratoires).
Condition de prescription
liste I
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Important
Présentation : 1 cartouche(s) polyéthylène polypropylène de 60 bouffées avec 1 inhalateur réutilisable
Prix : 23.76
Taux de remboursement : 65%
Titulaire : BOEHRINGER INGELHEIM INTERNATIONAL