TIOTROPIUM BIOGARAN EOLIP 18 microgrammes, poudre pour inhalation en gélule
Classe médicamenteuse
Autres médicaments pour les syndromes obstructifs des voies aériennes par inhalation, anticholinergiques | code ATC : R03BB04
Composition
Bromure de tiotropium amorphe.......................................................................... 21,7 microgrammes
Equivalant à tiotropium.......................................................................................... 18 microgrammes
Pour une gélule.
La dose délivrée à l’embout buccal de l’inhalateur est de 10 microgrammes de tiotropium.
Excipient à effet notoire :
Chaque gélule contient 5,2 milligrammes de lactose (correspondant à 5,5 milligrammes de lactose monohydraté).
Indications thérapeutiques
Le tiotropium est indiqué comme traitement bronchodilatateur continu destiné à soulager les symptômes des patients présentant une bronchopneumopathie chronique obstructive (BPCO).
Posologie et mode d'administration
Posologie
Ce médicament est destiné à une utilisation par voie inhalée exclusivement.
La posologie recommandée de bromure de tiotropium est l’inhalation du contenu d’une gélule une fois par jour à heure fixe dans la journée à l’aide de l’inhalateur à poudre sèche.
Ne pas dépasser la dose recommandée.
Les gélules de bromure de tiotropium sont destinées à l’inhalation exclusivement, et non à la voie orale. Ne pas avaler les gélules de bromure de tiotropium.
Le bromure de tiotropium est à inhaler uniquement à l’aide de l’inhalateur à poudre sèche MRX003-T10 / EOLIP.
Populations particulières
Sujets âgés
Le bromure de tiotropium peut être utilisé chez les sujets âgés à la dose recommandée.
Insuffisance rénale
Chez les patients atteints d'insuffisance rénale, le bromure de tiotropium peut être utilisé à la dose recommandée. En cas d'insuffisance rénale modérée à sévère (clairance de la créatinine ≤ 50 ml/min) voir rubriques 4.4 et 5.2.
Insuffisance hépatique
Le bromure de tiotropium peut être utilisé à la dose recommandée chez les patients atteints d'insuffisance hépatique (voir rubrique 5.2)
Population pédiatrique
BPCO
Il n’y a pas de justification à l’utilisation dans la population pédiatrique (patients de moins de 18 ans) dans l’indication mentionnée à la rubrique 4.1.
Mucoviscidose
La sécurité et l’efficacité de TIOTROPIUM BIOGARAN EOLIP 18 microgrammes chez les enfants et les adolescents n’ont pas été établies dans cette indication. Aucune étude n’est disponible.
Mode d’administration/Instructions pour la manipulation et l’utilisation
Pour une administration correcte du médicament, un médecin ou un autre professionnel de santé devra éduquer le patient au bon usage de l’inhalateur.
L’inhalateur à poudre sèche MRX003-T10 / EOLIP est exclusivement conçu pour l’administration des gélules TIOTROPIUM BIOGARAN EOLIP ; les patients ne doivent pas l’utiliser pour prendre un autre médicament.
La boite contient les gélules de TIOTROPIUM BIOGARAN EOLIP et, selon les présentations, contient également un inhalateur à poudre sèche (MRX003-T10 / EOLIP). Chaque inhalateur doit être remplacé après l’administration de 180 gélules et, pour cette raison, toutes les boites ne contiennent pas un inhalateur. Le dispositif ne doit pas être utilisé s’il présente des signes visibles de détérioration ou s’il reste une gélule à l’intérieur.
|
|
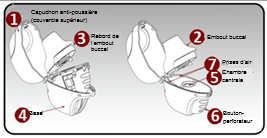
L’inhalateur à poudre sèche inclut : 1 Capuchon anti-poussière (couvercle supérieur) 2 Embout buccal 3 Rebord de l’embout buccal 4 Base 5 Chambre centrale 6 Bouton-perforateur 7 Prises d‘air |
|
La prise de la dose journalière complète du médicament exige 4 étapes principales Etape 1. Ouverture de l’inhalateur à poudre sèche : |
|
|
|
Après avoir sorti l’inhalateur à poudre sèche de son emballage : - · Le capuchon anti-poussière (couvercle supérieur) doit être ouvert en tirant vers le haut. - · Le capuchon anti-poussière (couvercle supérieur) doit être complètement relevé pour découvrir l’embout buccal. |
|
|
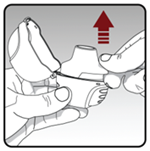
- · L’embout buccal doit être relevé en le tirant par le rebord vers le haut pour découvrir la chambre centrale. |
|
Etape 2. Insertion de la gélule dans l’inhalateur à poudre sèche : |
|
|
|
Une gélule doit être sortie de la plaquette (juste avant l’utilisation ; la gélule doit être utilisée dans les 30 minutes qui suivent, voir les instructions relatives à la manipulation de la plaquette). La gélule doit être placée dans la chambre centrale de l’inhalateur à poudre sèche. Le sens dans lequel la gélule est placée dans la chambre centrale importe peu. |
|
|
L’embout buccal doit être bien refermé dans la base jusqu’à entendre un clic. Le capuchon anti-poussière (couvercle supérieur) doit être laissé ouvert. |
|
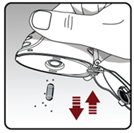
Etape 3. Perforation de la gélule : |
|
|
|
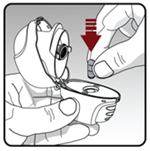
- L’inhalateur à poudre sèche doit être tenu avec l’embout buccal dirigé vers le haut. - Le bouton-perforateur doit être complètement enfoncé d’une seule pression vers l’intérieur jusqu’à l’arrêt, puis relâché. Ceci perfore la gélule et libère le médicament qui sera délivré lors de l’inhalation. - · Le bouton-perforateur ne doit pas être pressé plus d’une fois. - · L’inhalateur doit être tenu en position verticale. - · L’inhalateur à poudre sèche ne doit pas être agité. |
|
Etape 4. Prise de la dose complète journalière (2 inhalations à partir d’une seule gélule) : |
|
|
|
Le patient doit expirer à fond en 1 seule fois pour éliminer l’air des poumons. Important : le patient ne doit pas souffler dans l’inhalateur à poudre sèche. |
|
|
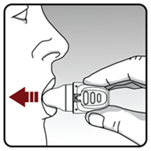
Le médicament doit être pris lors de l’inspiration suivante : - · La tête du patient doit être maintenue droite et il doit regarder droit devant lui. - · L’inhalateur à poudre sèche doit être porté à la bouche en position horizontale. Les prises d’air ne doivent pas être obstruées. - · Les lèvres doivent être fermement refermées autour de l’embout buccal. - · Le patient doit inspirer lentement et profondément jusqu’à remplir complètement les poumons et entendre et/ou sentir la gélule vibrer (cliqueter). - · La respiration doit être retenue pendant quelques secondes et, en même temps, l’inhalateur à poudre sèche doit être ôté de la bouche. - · Le patient doit reprendre une respiration normale. L’étape 4 doit être répétée une fois, ce qui videra totalement la gélule de son contenu. Important : le bouton-perforateur ne doit pas être pressé à nouveau. A retenir : pour obtenir la dose complète du médicament chaque jour, le patient doit inhaler 2 fois la même gélule. Le patient doit expirer à fond avant chaque inspiration à partir de l’inhalateur. Le patient ne doit pas souffler dans l’inhalateur à poudre sèche. |
|
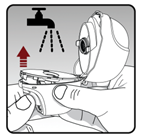
Nettoyage et conservation de l’inhalateur à poudre sèche : |
|
|
|
Après la prise de la dose journalière, l’embout buccal doit être ouvert et la gélule usagée doit être jetée à la poubelle. - · Tous les bouts de gélule ou la poudre restante doivent être éliminés en retournant l’inhalateur à poudre sèche et en tapant dessus doucement, mais fermement. L’embout buccal et le capuchon anti-poussière doivent ensuite être refermés. L’inhalateur à poudre sèche doit être conservé à température ambiante (ne dépassant pas 30 °C). L’inhalateur à poudre sèche doit être nettoyé une fois par mois. Après nettoyage, le séchage à l’air de l’inhalateur à poudre sèche prend 24 heures. - · Aucun agent de nettoyage ou détergent ne doit être utilisé. - L’inhalateur à poudre sèche ne doit pas être placé dans le lave-vaisselle pour être nettoyé. Etapes de nettoyage - · Le capuchon anti-poussière et l’embout buccal doivent être ouverts. - · La base doit être ouverte en soulevant le bouton-perforateur. - · Le patient doit regarder dans la chambre centrale pour vérifier s’il n’y a pas de bouts de gélule ou de poudre restante. Si c’est le cas, il faut secouer pour les enlever. - · L’inhalateur à poudre sèche doit être rincé à l’eau chaude et le bouton doit être pressé plusieurs fois pour que la chambre centrale et l’aiguille de perforation soient sous l’eau courante. Il faut vérifier que toute la poudre et les bouts de gélules soient éliminés. - · L’inhalateur à poudre sèche doit être séché soigneusement en absorbant l’excès d’eau sur une serviette en papier. Il doit ensuite être séché à l’air, en laissant le capuchon anti-poussière, l’embout buccal et la base ouverts, en l’étalant complètement pour qu’il sèche entièrement. - · Un sèche-cheveux ne doit pas être utilisé pour sécher l’inhalateur à poudre sèche. - L’inhalateur à poudre sèche ne doit pas être utilisé lorsqu’il est mouillé. Si nécessaire, la surface externe de l’embout buccal doit être nettoyée à l’aide d’un chiffon humide. |
|
Manipulation de la plaquette |
|
|
|
Chaque jour, 1 seule alvéole doit être séparée de la plaquette prédécoupée unitaire en détachant selon la perforation. |
|
|
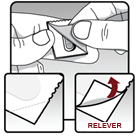
La gélule doit être sortie de la plaquette : - · La feuille ne doit pas être coupée. Aucun instrument pointu ne doit être utilisé pour retirer la gélule de la plaquette. - · Les patients doivent plier l’un des angles de l’alvéole en direction de la flèche. - · La feuille d‘aluminium doit être relevée (juste avant l’utilisation) progressivement jusqu’à ce que la gélule devienne complètement visible. Si une seconde gélule est exposée à l’air par inadvertance, celle-ci ne doit pas être utilisée et doit être jetée. |
|
|
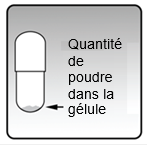
Chaque gélule ne contient qu’une petite quantité de poudre. Cela correspond à 1 dose complète. |
Voie d'administration
inhalée
Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1 ou à l’atropine ou ses dérivés, tels que l’ipratropium ou l’oxitropium.
Mise en garde et précautions d'emploi
Le bromure de tiotropium est un traitement bronchodilatateur continu de longue durée d’action en une prise par jour et ne doit pas être utilisé comme un médicament de secours de première intention pour le traitement de secours des épisodes aigus de bronchospasme.
Des réactions d’hypersensibilité immédiate peuvent apparaître après l’administration de bromure de tiotropium sous forme de poudre pour inhalation.
Compte tenu de son activité anticholinergique, le bromure de tiotropium doit être utilisé avec prudence en cas de glaucome à angle fermé, d’hypertrophie de la prostate ou de rétrécissement du col de la vessie (voir rubrique 4.8).
D’une façon générale, l’administration de médicaments par voie inhalée est susceptible de déclencher un bronchospasme.
Le tiotropium doit être utilisé avec prudence chez les patients ayant eu un infarctus du myocarde au cours des six derniers mois, ou une arythmie cardiaque instable ou engageant le pronostic vital ou une arythmie cardiaque nécessitant une intervention ou un changement de thérapie au cours de l’année précédente ; ou chez les patients ayant été hospitalisés pour une insuffisance cardiaque (NYHA classe III ou IV) au cours de l’année précédente. Ces patients ont été exclus des essais cliniques et ces maladies peuvent être affectées par le mécanisme d’action des anticholinergiques.
Les concentrations plasmatiques de bromure de tiotropium augmentent en cas d’altération de la fonction rénale. Par conséquent, chez les patients atteints d’insuffisance rénale modérée à sévère (clairance de la créatinine ≤ 50 mL/min), le bromure de tiotropium ne doit être utilisé que si le bénéfice attendu dépasse le risque potentiel. A ce jour il n’y a pas d’expérience à long terme chez les patients souffrant d’insuffisance rénale sévère (voir rubrique 5.2).
Il faut avertir les patients d’éviter la projection de la poudre contenue dans la gélule dans les yeux. Il conviendra de les informer du risque de déclenchement ou d’aggravation d’un glaucome à angle fermé, de douleur ou de gêne oculaire, de vision floue transitoire avec halo visuel coloré associé à une rougeur et un œdème cornéo-conjonctival en cas de projection intraoculaire de la poudre. Si une combinaison quelconque de ces symptômes oculaires apparaît, les patients doivent interrompre immédiatement l’utilisation du bromure de tiotropium et consulter immédiatement un médecin ophtalmologue.
La sécheresse buccale observée avec les traitements anticholinergiques, peut à long terme favoriser la survenue de caries dentaires.
La posologie du bromure de tiotropium ne doit pas dépasser une prise par jour (voir rubrique 4.9).
Les gélules TIOTROPIUM BIOGARAN EOLIP contiennent 5,2 mg de lactose (ce qui correspond à 5,5 mg de lactose monohydraté). Cette quantité ne provoque habituellement pas de problèmes chez les patients intolérants au lactose. Les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose et du galactose (maladies héréditaires rares) ne doivent pas prendre ce médicament. Le lactose est un excipient qui peut contenir des petites quantités de protéine de lait qui peuvent entraîner des réactions allergiques.
Condition de prescription
liste I
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Important
Présentation : 3 plaquettes prédécoupées unitaires aluminium PVC-Aluminium de 10 gélule(s) avec inhalateur
Prix : non disponible
Taux de remboursement : 0%
Titulaire : BIOGARAN