EPREX 4000 UI/mL, solution injectable en seringue préremplie
Classe médicamenteuse
Antianémique. | Code ATC : B03XA01
Composition
Epoétine alfa...................................................................... 4000 UI/mL (33,6 microgrammes par mL)
produite sur cellules ovariennes de hamster chinois (CHO) par la technique de l’ADN recombinant.
Une seringue préremplie de 0,5 mL contient 2000 UI (16,8 microgrammes) d’époétine alfa.
Indications thérapeutiques
EPREX est indiqué dans le traitement de l’anémie symptomatique associée à une insuffisance rénale chronique (IRC) :
- chez les adultes et les enfants âgés de 1 à 18 ans hémodialysés et chez les patients adultes en dialyse péritonéale,
- chez les adultes insuffisants rénaux non encore dialysés pour le traitement de l'anémie sévère d'origine rénale accompagnée de symptômes cliniques chez les patients.
EPREX est indiqué chez les adultes traités par chimiothérapie pour des tumeurs solides, un lymphome malin ou un myélome multiple, et à risque de transfusion en raison de leur état général (par exemple, état cardiovasculaire, anémie pré‑existante au début de la chimiothérapie) pour le traitement de l'anémie et la réduction des besoins transfusionnels.
EPREX est indiqué chez les adultes participant à un programme de transfusions autologues différées pour augmenter les dons de sang autologue. Le traitement doit être uniquement administré aux patients présentant une anémie modérée (concentration d’hémoglobine comprise entre 10 et 13 g/dL [soit 6,2 - 8,1 mmol/L], sans carence martiale) s’il n’existe pas ou peu de méthodes d’épargne du sang lorsqu’une intervention chirurgicale majeure programmée nécessite de grandes quantités de sang (4 unités de sang ou plus chez les femmes et 5 unités de sang ou plus chez les hommes).
EPREX est indiqué chez les adultes, sans carence martiale, devant avoir une intervention chirurgicale orthopédique majeure programmée, ayant un risque présumé important de complications transfusionnelles pour réduire l'exposition aux transfusions de sang homologue. L'utilisation devra être réservée aux patients ayant une anémie modérée (par exemple, concentration d’hémoglobine comprise entre 10 et 13 g/dL) qui n'ont pas accès à un programme de transfusions autologues différées et chez lesquels on s’attend à des pertes de sang modérées (900 à 1800 mL).
EPREX est indiqué pour le traitement de l’anémie symptomatique (concentration d’hémoglobine ≤ 10 g/dL) chez les adultes atteints de syndromes myélodysplasiques (SMD) primitifs de risque faible ou intermédiaire 1, présentant un taux sérique d’érythropoïétine faible (< 200 mU/mL).
Posologie et mode d'administration
Posologie
Toutes les autres causes d’anémie (carences en fer, folates ou vitamine B12, intoxication à l’aluminium, infection ou inflammation, pertes sanguines, hémolyse et fibrose médullaire quelle qu’en soit l’origine) doivent être évaluées et traitées avant d’instaurer un traitement par époétine alfa, et de décider d’augmenter la posologie. Pour garantir une réponse optimale à l’époétine alfa, des réserves en fer suffisantes doivent être assurées et une supplémentation en fer doit être administrée si besoin (voir rubrique 4.4).
Traitement de l’anémie symptomatique chez les patients adultes en insuffisance rénale chronique :
Les symptômes et conséquences de l’anémie peuvent varier avec l’âge, le sexe et les comorbidités ; une évaluation par le médecin de l’état de santé et de l’évolution clinique du patient est nécessaire.
L’intervalle recommandé pour la concentration d’hémoglobine désirée est compris entre 10 g/dLl et 12 g/dL (6,2 à 7,5 mmol/L). EPREX doit être administré afin d’augmenter l’hémoglobine à un taux ne dépassant pas 12 g/dL (7,5 mmol/L). Une augmentation du taux d’hémoglobine supérieure à 2 g/dL (1,25 mmol/L) sur une période de quatre semaines doit être évitée. Si cela se produit, une adaptation appropriée de la dose doit être réalisée comme indiqué.
En raison de la variabilité intra-patient, des valeurs individuelles et occasionnelles du taux d’hémoglobine au-dessus et au-dessous de l’intervalle de concentrations d’hémoglobine désiré peuvent être observées chez un même patient. La variabilité du taux d’hémoglobine doit être prise en compte par l’adaptation de la posologie en tenant compte de l’intervalle de la concentration d’hémoglobine allant de 10 g/dL (6,2 mmol/L) à 12 g/dL (7,5 mmol/L).
Un taux d’hémoglobine prolongé supérieur à 12 g/dL (7,5 mmol/L) doit être évité. Si le taux d’hémoglobine augmente de plus de 2 g/dL (1,25 mmol/L) par mois, ou si le taux d’hémoglobine prolongé dépasse 12 g/dL (7,5 mmol/L), réduire la dose d’EPREX de 25 %. Si le taux d’hémoglobine dépasse 13 g/dL (8,1 mmol/L), interrompre le traitement jusqu’à ce que le taux s’abaisse en dessous de 12 g/dL (7,5 mmol/L) et reprendre le traitement par EPREX à une dose de 25 % inférieure à la dose précédente.
Les patients doivent être étroitement surveillés afin de s’assurer que la dose d’EPREX efficace la plus faible soit utilisée pour obtenir un contrôle adéquat de l’anémie et des symptômes de l’anémie tout en maintenant une concentration d’hémoglobine inférieure ou égale à 12 g/dL (7,5 mmol/L).
La prudence s’impose en cas d’augmentation de dose de l’ASE (Agent Stimulant l’Erythropoïèse) chez les patients ayant une insuffisance rénale chronique. Chez les patients ayant une réponse faible aux ASE, d’autres facteurs expliquant la faible réponse devront être considérés (voir rubriques 4.4 et 5.1).
Le traitement par EPREX est divisé en deux phases : une phase correctrice et une phase d’entretien.
Patients adultes en hémodialyse
Chez les patients en hémodialyse, lorsque la voie intraveineuse est déjà disponible, l’administration par la voie intraveineuse est préférable.
- Phase correctrice
La posologie initiale est de 50 UI/kg 3 fois par semaine.
Si nécessaire, augmenter ou diminuer la dose de 25 UI/kg (3 fois par semaine) jusqu’à atteindre l’intervalle de concentrations d’hémoglobine désiré, compris entre 10 g/dL et 12 g/dL (6,2 mmol/L à 7,5 mmol/L) (ceci doit être réalisé par palier d'au moins 4 semaines).
- Phase d'entretien
La dose totale recommandée par semaine est comprise entre 75 UI/kg et 300 UI/kg.
Une adaptation appropriée de la dose devra être réalisée pour maintenir les valeurs de l’hémoglobine dans l’intervalle de concentrations désiré, compris entre 10 g/dL et 12 g/dL (6,2 à 7,5 mmol/L).
Les patients avec un taux d'hémoglobine à l’instauration très bas (< 6 g/dL ou < 3,75 mmol/L) peuvent avoir besoin de doses d'entretien plus élevées que les patients dont l'anémie à l’instauration est moins sévère (> 8 g/dL ou > 5 mmol/L).
Patients adultes insuffisants rénaux non encore dialysés
Lorsque la voie intraveineuse n’est pas encore disponible, EPREX peut être administré par voie sous-cutanée.
La posologie initiale est de 50 UI/kg 3 fois par semaine, suivie si nécessaire d'une augmentation de dose de 25 UI/kg (3 fois par semaine) jusqu'à atteindre le but désiré (ceci doit être réalisé par palier d'au moins 4 semaines).
Lors de la phase d’entretien, EPREX peut être administré 3 fois par semaine ou, dans le cas d’une administration par voie sous-cutanée, une fois par semaine ou une fois toutes les deux semaines.
Une adaptation appropriée de la dose et de l’intervalle d’administration devra être réalisée pour maintenir les valeurs de l'hémoglobine au taux désiré : hémoglobine entre 10 g/dL et 12 g/dL (6,2 à 7,5 mmol/L). Une prolongation de l’intervalle d’administration peut nécessiter une augmentation de la dose.
La posologie maximale ne doit pas excéder 150 UI/kg 3 fois par semaine, 240 UI/kg (jusqu’à un maximum de 20 000 UI) une fois par semaine, ou 480 UI/kg (jusqu’à un maximum de 40 000 UI) une fois toutes les deux semaines.
Patients adultes en dialyse péritonéale
Lorsque la voie intraveineuse n’est pas encore disponible, EPREX peut être administré par voie sous-cutanée.
La posologie initiale est de 50 UI/kg 2 fois par semaine.
La dose d’entretien recommandée est comprise entre 25 UI/kg et 50 UI/kg, 2 fois par semaine en 2 injections identiques.
Une adaptation appropriée de la dose devra être réalisée pour maintenir les valeurs de l'hémoglobine au taux désiré, entre 10 g/dL et 12 g/dL (6,2 à 7,5 mmol/L).
Traitement des patients adultes ayant une anémie induite par la chimiothérapie
Les symptômes et conséquences de l’anémie peuvent varier avec l’âge, le sexe et l’impact global de la maladie ; une évaluation par le médecin de l’état de santé et de l’évolution clinique du patient est nécessaire.
EPREX doit être administré aux patients ayant une anémie (par exemple, une concentration d’hémoglobine ≤ 10 g/dL (6,2 mmol/L)).
La dose initiale est de 150 UI/kg administrée par voie sous-cutanée 3 fois par semaine.
Alternativement, EPREX peut être administré par voie sous-cutanée à la dose initiale de 450 UI/kg une fois par semaine.
Une adaptation appropriée de la dose devra être réalisée pour maintenir les valeurs de l'hémoglobine dans l’intervalle de concentrations désiré, compris entre 10 g/dL et 12 g/dL (6,2 à 7,5 mmol/L).
En raison de la variabilité intra-patient, des concentrations individuelles et occasionnelles du taux d’hémoglobine au-dessus et au-dessous de l’intervalle de concentrations d’hémoglobine désiré peuvent être observées chez un même patient. La variabilité du taux d’hémoglobine doit être prise en compte par l’adaptation de la posologie en tenant compte de l’intervalle de concentrations d’hémoglobine désiré, compris entre 10 g/dL (6,2 mmol/L) et 12 g/dL (7,5 mmol/L). Une concentration d’hémoglobine prolongée supérieure à 12 g/dL (7,5 mmol/L) doit être évitée ; des recommandations sur l’adaptation posologique appropriée lorsque les concentrations d’hémoglobine dépassent 12 g/dL (7,5 mmol/L) sont décrites ci-dessous.
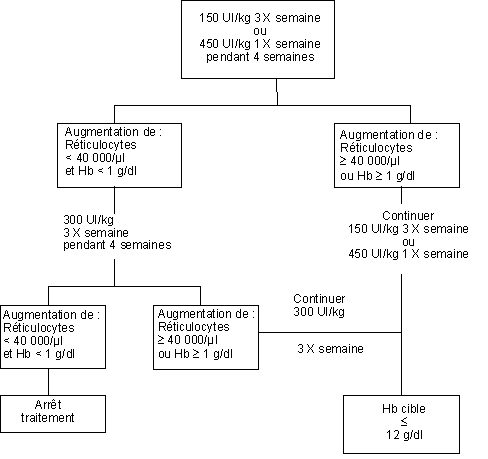
Si la concentration d'hémoglobine a augmenté d'au moins 1 g/dL (0,62 mmol/L), ou si le nombre de réticulocytes a augmenté d’au moins 40 000 cellules/µL par rapport aux valeurs initiales après 4 semaines de traitement, la dose doit être maintenue à 150 UI/kg 3 fois par semaine ou 450 UI/kg 1 fois par semaine.
Si l'augmentation de la concentration d'hémoglobine est inférieure à 1 g/dL (inférieure à 0,62 mmol/L) et si le nombre de réticulocytes a augmenté de moins de 40 000 cellules/µL par rapport aux valeurs initiales, augmenter la dose à 300 UI/kg 3 fois par semaine. Si après 4 semaines supplémentaires de traitement à 300 UI/kg 3 fois par semaine, la concentration d'hémoglobine a augmenté d’au moins 1 g/dL (au moins 0,62 mmol/L) ou le nombre de réticulocytes a augmenté d’au moins 40 000 cellules/µL, la dose de 300 UI/kg 3 fois par semaine doit être maintenue.
Si la concentration d'hémoglobine a augmenté de moins de 1 g/dL (moins de 0,62 mmol/L) et le nombre de réticulocytes a augmenté de moins de 40 000 cellules/µL par rapport aux valeurs initiales, la réponse est improbable et le traitement doit être arrêté.
Adaptation de la posologie pour maintenir les concentrations d’hémoglobine entre 10 g/dL et 12 g/dL
Si la concentration d’hémoglobine augmente de plus de 2 g/dL (1,25 mmol/L) par mois, ou si la concentration d’hémoglobine dépasse 12 g/dL (7,5 mmol/L), réduire la dose d’EPREX d’environ 25 % à 50 %.
Si la concentration d’hémoglobine dépasse 13 g/dL (8,1 mmol/L), interrompre le traitement jusqu’à ce que la concentration baisse en dessous de 12 g/dL (7,5 mmol/L) et reprendre le traitement par EPREX à une dose de 25 % inférieure à la dose précédente.
![]()
![]()
![]() Le schéma posologique recommandé est décrit ci-après :
Le schéma posologique recommandé est décrit ci-après :
 |
Les patients doivent être étroitement surveillés afin de s’assurer que la dose d’Agent Stimulant l’Erythropoïèse (ASE) la plus faible soit utilisée pour obtenir un contrôle adéquat des symptômes de l’anémie.
Le traitement par EPREX doit être poursuivi jusqu’à un mois après l’arrêt de la chimiothérapie.
Traitement des patients adultes en chirurgie participant à un programme de transfusions autologues différées
La posologie d'EPREX chez les patients ayant une anémie modérée (hématocrite entre 33 et 39 %) qui doivent donner au moins 4 unités de sang, est de 600 UI/kg par voie intraveineuse 2 fois par semaine pendant 3 semaines avant l'intervention. EPREX doit être administré après la fin de procédure du don de sang.
Traitement des patients adultes devant avoir une chirurgie orthopédique majeure programmée
La dose recommandée d’EPREX est de 600 UI/kg administrée par voie sous-cutanée une fois par semaine pendant les 3 semaines (jour -21, -14, -7) précédant l'intervention chirurgicale et le jour de l'intervention.
Si pour des raisons médicales la période avant l'intervention doit être réduite à moins de 3 semaines, EPREX doit être administré par voie sous-cutanée à la dose de 300 UI/kg tous les jours, pendant 10 jours consécutifs avant l'intervention, le jour de l'intervention et pendant les 4 jours suivant l'intervention.
Si la concentration d'hémoglobine atteint 15 g/dL ou plus pendant la période pré-opératoire, l'administration d'EPREX doit être arrêtée et les doses ultérieures initialement prévues ne doivent pas être administrées.
Traitement des patients adultes atteint d’un SMD de risque faible ou intermédiaire 1
EPREX doit être administré aux patients présentant une anémie symptomatique (i.e. concentration d’hémoglobine ≤10 g/dL (6.2 mmol/L)).
La dose initiale recommandée d’EPREX est de 450 UI/kg (la dose totale maximale est de 40 000 UI) administrée par voie sous-cutanée 1 fois chaque semaine, avec un espacement des doses d’au moins 5 jours.
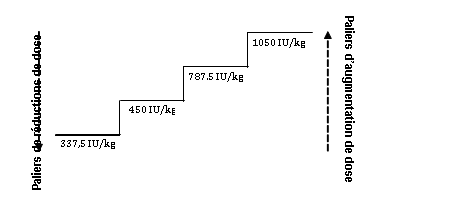
Des ajustements appropriés de doses doivent être appliqués afin de maintenir des concentrations d’hémoglobine comprises dans l’intervalle cible de 10 g/dL à 12 g/dL (6.2 à 7.5 mmol/L). Il est recommandé d’évaluer la réponse érythroïde 8 à 12 semaines suivant l’initiation du traitement. Les augmentations et diminutions de dose doivent être faites par paliers de dose successifs (voir diagramme ci-dessous). Une concentration en hémoglobine supérieure à 12 g/dL (7.5 mmol/L) doit être évitée.
Augmentation de dose : la dose ne doit pas être augmentée au-delà de 1050 UI/kg (dose totale de 80 000 UI) par semaine. Si le patient perd la réponse ou que la concentration en hémoglobine chute de ≥ 1 g/dL après la réduction de dose, celle-ci doit être augmentée d’un palier de dose. Un délai minimum de 4 semaines doit être respecté entre les augmentations de dose.
Suspension et diminution de dose : l'époétine alfa doit être suspendue lorsque la concentration d'hémoglobine dépasse 12 g/dL (7,5 mmol/L). Une fois que le taux d'hémoglobine est < 11 g/dL, la dose peut être redémarrée sur le même palier de dose ou sur un palier inférieur selon l’évaluation du médecin. Une diminution de dose en une seule étape peut être envisagée s'il y a une augmentation rapide du taux d'hémoglobine (> 2 g/dL sur 4 semaines).
Les symptômes et les séquelles de l'anémie peuvent varier en fonction de l'âge, du sexe et des comorbidités. Une évaluation individuelle de l'état du patient et du traitement par le médecin est nécessaire.
Population pédiatrique
Traitement de l’anémie symptomatique chez les patients insuffisants rénaux chroniques hémodialysés
Les symptômes et conséquences de l’anémie peuvent varier avec l’âge, le sexe et les co-morbidités ; une évaluation par le médecin de l’état de santé et de l’évolution clinique du patient est nécessaire.
Chez les enfants, l’intervalle de concentrations d’hémoglobine recommandé est compris entre 9,5 g/dL et 11 g/dL (5,9 et 6,8 mmol/L). EPREX doit être administré afin d’augmenter l’hémoglobine à un taux ne dépassant pas 11 g/dL (6,8 mmol/L). Une augmentation du taux d’hémoglobine supérieure à 2 g/dL (1,25 mmol/L) sur une période de quatre semaines doit être évitée. Si cela se produit, une adaptation appropriée de la dose doit être réalisée comme indiqué.
Les patients doivent être étroitement surveillés afin de s’assurer que la dose d’EPREX la plus faible soit utilisée pour obtenir un contrôle adéquat de l’anémie et des symptômes de l’anémie.
Chez les enfants hémodialysés, lorsque la voie intraveineuse est déjà disponible, l’administration par la voie intraveineuse est préférable.
La posologie initiale est de 50 UI/kg 3 fois par semaine par voie intraveineuse.
Si nécessaire, augmenter ou diminuer la dose de 25 UI/kg (3 fois par semaine) jusqu'à atteindre l’intervalle de concentrations d’hémoglobine désiré, compris entre 9,5 g/dL et 11 g/dL (5,9 à 6,8 mmol/L) (ceci doit être réalisé par palier d’au moins 4 semaines).
Une adaptation appropriée de la dose devra être réalisée afin de maintenir un taux d’hémoglobine dans l’intervalle de concentrations désiré, compris entre 9,5 g/dL et 11 g/dL (5,9 et 6,8 mmol/L).
Généralement les enfants de moins de 30 kg nécessitent des doses d’entretien plus importantes que ceux de plus de 30 kg et que les adultes.
Les enfants avec un taux d'hémoglobine à l’instauration très bas (< 6,8 g/dL ou < 4,25 mmol/L) peuvent avoir besoin de doses d'entretien plus importantes que ceux dont le taux d'hémoglobine à l’instauration est plus élevé (> 6,8 g/dL ou > 4,25 mmol/L).
Anémie chez les patients insuffisants rénaux chroniques avant l’instauration de la dialyse ou en dialyse péritonéale
La sécurité et l’efficacité d’EPREX chez les patients insuffisants rénaux chroniques et anémiés, avant l’instauration de la dialyse ou étant en dialyse péritonéale, n’ont pas encore été établies. Les données actuellement disponibles concernant l’utilisation d’EPREX par voie sous-cutanée dans ces populations sont décrites dans la rubrique 5.1 mais aucune recommandation posologique ne peut être donnée.
Traitement des enfants ayant une anémie induite par la chimiothérapie
La sécurité et l’efficacité d’EPREX chez les enfants recevant une chimiothérapie n’ont pas encore été établies (voir rubrique 5.1).
Traitement des enfants en chirurgie participant à un programme de transfusions autologues différées
La sécurité et l’efficacité d’EPREX chez les enfants n’ont pas encore été établies. Aucune donnée n’est disponible.
Traitement des enfants devant avoir une chirurgie orthopédique majeure programmée
Mode d’administration
Précautions à prendre avant la manipulation et l’administration du médicament :
Avant utilisation, laisser reposer la seringue d’EPREX jusqu’à ce qu’elle atteigne la température ambiante. Ceci prend habituellement 15 à 30 minutes.
Traitement de l’anémie symptomatique chez les patients adultes insuffisants rénaux chroniques
Chez les patients en insuffisance rénale chronique dont l’accès à la voie intraveineuse est déjà disponible (patients hémodialysés), l’administration d’EPREX par voie intraveineuse est préférable.
Lorsque l’accès à la voie intraveineuse n’est pas encore disponible (patients non encore dialysés et patients en dialyse péritonéale), EPREX peut être administré par injection sous-cutanée.
Traitement des patients adultes ayant une anémie induite par la chimiothérapie
EPREX doit être administré par injection sous-cutanée.
Traitement des patients adultes en chirurgie participant à un programme de transfusions autologues différées
EPREX doit être administré par voie intraveineuse.
Traitement des patients adultes devant avoir une chirurgie orthopédique majeure programmée
Traitement des patients adultes atteints de SMD de risque faible ou intermédiaire 1
Traitement de l’anémie symptomatique chez les enfants insuffisants rénaux chroniques hémodialysés
Chez les enfants en insuffisance rénale chronique dont l’accès à la voie intraveineuse est déjà disponible (patients hémodialysés), l’administration d’EPREX par voie intraveineuse est préférable.
Administration intraveineuse
Administrer en une à cinq minutes au moins, selon la dose totale. Chez les patients en hémodialyse, une injection en bolus peut être réalisée pendant la séance de dialyse dans le site d'injection approprié situé au niveau du retour veineux de la ligne de dialyse. Autrement, l’injection peut être faite à la fin de la séance de dialyse dans l'aiguille à fistule, en la faisant suivre d'un rinçage par 10 mL de solution saline isotonique afin d'assurer le bon passage du produit dans la circulation.
Une administration plus lente est préférable chez les patients qui auraient présenté des symptômes pseudo‑grippaux (voir rubrique 4.8).
Ne pas administrer EPREX en perfusion intraveineuse, ni en mélange avec d'autres solutions de médicaments.
Administration sous-cutanée
Un volume maximal de 1 mL par site d'injection ne doit généralement pas être dépassé. En cas de volume plus important, utiliser plus d'un site pour l'injection.
Les injections se font au niveau des membres ou de la paroi abdominale antérieure.
Dans le cas où le médecin décide que le patient ou le personnel soignant peut administrer EPREX par voie sous-cutanée de manière sûre et efficace, des instructions pour un bon dosage et une bonne administration doivent être fournies.
Comme avec les autres médicaments injectables, assurez-vous de l’absence de particules dans la solution ou d’un changement de couleur.
Marques de graduation
L'étiquette de la seringue contient des marques de graduation numérotées afin de permettre l'administration d'une partie de la dose (voir rubrique 6.6). Cependant, le produit est à usage unique seulement. Une seule dose d'EPREX doit être utilisée pour chaque seringue.
Voie d'administration
intraveineuse;sous-cutanée
Contre-indications
- Hypersensibilité à la substance active ou à l'un des excipients mentionnés à la rubrique 6.1.
- Les patients ayant développé une érythroblastopénie à la suite d'un traitement par une érythropoiétine ne doivent pas être traités par EPREX ou par toute autre érythropoiétine (voir rubrique 4.4 - Erythroblastopénie).
- Hypertension non contrôlée.
- Toutes les contre-indications associées à un programme de transfusions autologues différées doivent être respectées chez les patients qui reçoivent EPREX au cours d'un tel programme.
- L'utilisation d'EPREX, chez les patients devant avoir une intervention chirurgicale orthopédique majeure programmée et ne participant pas à un programme de transfusions autologues différées, est contre‑indiquée chez les patients présentant une pathologie vasculaire sévère coronarienne, des artères périphériques, carotidienne, ou cérébrales, y compris chez les patients présentant des antécédents récents d'infarctus du myocarde ou d'accident vasculaire cérébral.
- Les patients en chirurgie qui, quelle qu'en soit la raison, ne peuvent pas recevoir une prophylaxie antithrombotique appropriée.
Mise en garde et précautions d'emploi
Traçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Généralités
Chez tous les patients traités par époétine alfa, la pression artérielle doit être suivie étroitement et contrôlée de façon appropriée. Epoétine alfa doit être utilisée avec précaution en présence d'une hypertension non ou insuffisamment traitée ou difficilement contrôlable. Il peut être nécessaire d’instaurer ou d'augmenter le traitement anti‑hypertenseur. Si la pression artérielle ne peut être contrôlée, le traitement par époétine alfa doit être interrompu.
Des crises hypertensives avec encéphalopathie et convulsions, nécessitant l'attention immédiate d'un médecin et la prise en charge en soins intensifs, sont également survenues pendant le traitement par époétine alfa chez des patients dont la pression artérielle était précédemment normale ou basse. Une attention particulière devra être accordée aux céphalées violentes pseudo-migraineuses d’apparition brutale, comme un possible signal d'alarme (voir rubrique 4.8).
L’époétine alfa doit être utilisée avec précaution chez les patients épileptiques, ayant des antécédents de convulsions, ou ayant des pathologies associées à une prédisposition aux convulsions, comme les infections du SNC et les métastases cérébrales.
L’époétine alfa doit être utilisée avec précaution chez les patients ayant une insuffisance hépatique chronique. La sécurité de l’époétine alfa n’a pas été établie chez les patients ayant un dysfonctionnement hépatique.
Une augmentation de l’incidence des événements vasculaires thrombotiques (EVT) a été observée chez les patients recevant des ASE (voir rubrique 4.8). Ces événements incluent les thromboses veineuses ou artérielles et les embolies (dont certaines avec une issue fatale), tels que thrombose veineuse profonde, embolie pulmonaire, thrombose rétinienne et infarctus du myocarde. En outre, des accidents vasculaires cérébraux (incluant infarctus cérébral, hémorragie cérébrale et accidents ischémiques transitoires) ont été rapportés.
Le risque rapporté d’EVT doit être soigneusement évalué au regard du bénéfice du traitement par époétine alfa, en particulier chez les patients ayant des facteurs de risque préexistants d’EVT, incluant obésité et antécédents d’EVT (par exemple, thrombose veineuse profonde, embolie pulmonaire, et accident vasculaire cérébral).
Chez tous les patients, les taux d’hémoglobine doivent être étroitement surveillés en raison du risque potentiel augmenté d’évènements thrombo-emboliques et d’évolutions fatales lorsque les patients sont traités à des taux d’hémoglobine supérieurs à l’intervalle de concentration correspondant à l’indication utilisée.
Lors d'un traitement par époétine alfa, une augmentation modérée et dose-dépendante de la numération plaquettaire, dans les limites de la normale, peut être observée. Celle-ci régresse avec la poursuite du traitement. De plus, des cas de thrombocytémie supérieurs au taux normal ont été rapportés. Il est conseillé de surveiller la numération plaquettaire à intervalles réguliers pendant les 8 premières semaines de traitement.
Toutes les autres causes d'anémie (carences en fer, folates ou vitamine B12, intoxication à l’aluminium, infection ou inflammation, pertes sanguines, hémolyse et fibrose médullaire quelle qu’en soit l’origine) doivent être évaluées et traitées avant d'instaurer le traitement par époétine alfa et de décider d’augmenter la posologie. Dans la plupart des cas, les taux de ferritine sérique chutent parallèlement à l'augmentation de l'hématocrite. Pour garantir une réponse optimale à l’époétine alfa, des réserves en fer suffisantes doivent être assurées et une supplémentation en fer doit être administrée si besoin (voir rubrique 4.2) :
- Pour les patients ayant une insuffisance rénale chronique, une supplémentation en fer (dose de fer élément par voie orale comprise entre 200 et 300 mg/jour chez les adultes, et entre 100 et 200 mg/jour chez les enfants) est recommandée si les taux de ferritine sérique sont inférieurs à 100 ng/mL.
- Pour les patients atteints d’un cancer, une supplémentation en fer (dose de fer élément par voie orale comprise entre 200 et 300 mg/jour) est recommandée si le coefficient de saturation de transferrine est inférieur à 20 %.
- Pour les patients participant à un programme de transfusions autologues différées, une supplémentation en fer (dose de fer élément de 200 mg/jour par voie orale) doit être administrée plusieurs semaines en amont de l’instauration du prélèvement autologue afin de constituer des réserves en fer élevées avant d’instaurer le traitement par époétine alfa, et pendant toute la durée du traitement par époétine alfa.
- Pour les patients devant avoir une intervention chirurgicale orthopédique majeure programmée, une supplémentation en fer (dose de fer élément de 200 mg/jour par voie orale) devra être administrée pendant toute la durée du traitement par époétine alfa. Si possible, la supplémentation en fer doit être instaurée avant de commencer le traitement par époétine alfa pour constituer des réserves en fer suffisantes.
L’apparition ou l’aggravation d’une porphyrie a été très rarement observée chez les patients traités par époétine alfa. L’époétine alfa doit être utilisée avec précaution chez les patients atteints de porphyrie.
Des réactions indésirables cutanées sévères (SCAR), dont le syndrome de Stevens-Johnson (SSJ) et le syndrome de Lyell, pouvant engager le pronostic vital ou être fatales ont été signalées dans le cadre de traitements à base d’époétine. Des cas plus graves ont été observés lors de l’utilisation d’époétines à longue durée d’action.
Au moment de la prescription, les patients doivent être informés des signes et symptômes et faire l’objet d’une surveillance étroite des réactions cutanées. Si des signes ou symptômes évoquant l’une de ces réactions apparaissent, EPREX doit être arrêté immédiatement et un traitement de substitution doit être envisagé.
Si le patient a développé une réaction cutanée sévère telle que le SSJ ou le syndrome de Lyell en raison de l’utilisation d’EPREX, il ne faut jamais réintroduire un traitement à base d’EPREX chez ce patient.
Le capuchon d’aiguille de la seringue préremplie contient du caoutchouc naturel sec (un dérivé du latex), qui peut provoquer de graves réactions allergiques chez les personnes sensibles au latex. Les patients ne peuvent voir leur traitement modifié d’un ASE à un autre que sous une surveillance adaptée.
Erythroblastopénies
Des érythroblastopénies avec anticorps ont été rapportées après plusieurs mois ou années de traitement par époétine alfa.
Des cas ont également été rapportés chez des patients atteints d’hépatite C et traités par interféron et ribavirine lors de l’utilisation concomitante d’ASE. L’époétine alfa n’est pas approuvée dans la prise en charge de l’anémie associée à une hépatite C.
Chez les patients présentant une perte soudaine d’efficacité définie par une baisse de l’hémoglobine (de 1 à 2 g/dL par mois) avec une augmentation des besoins transfusionnels, une numération des réticulocytes doit être réalisée et les causes habituelles de non réponse (carences en fer, folates ou vitamine B12, intoxication à l’aluminium, infection ou inflammation, pertes sanguines, hémolyse et fibrose médullaire quelle qu’en soit l’origine) doivent être recherchées.
Une diminution paradoxale du taux d’hémoglobine et le développement d’une anémie sévère associée à un faible taux de réticulocytes imposent l’arrêt immédiat du traitement par l’époétine alfa et une recherche des anticorps anti-érythropoïétine. Une ponction médullaire doit aussi être envisagée pour confirmer le diagnostic d’érythroblastopénie.
Aucun traitement par un autre ASE ne devra être débuté en raison du risque de réaction croisée.
Traitement de l’anémie symptomatique chez l’adulte et l’enfant en insuffisance rénale chronique :
Chez les patients en insuffisance rénale chronique traités par époétine alfa, les taux d'hémoglobine doivent être régulièrement mesurés jusqu'à ce qu'un taux stable soit atteint, puis périodiquement ensuite.
Chez les patients insuffisants rénaux chroniques, le taux d'hémoglobine doit augmenter d'environ 1 g/dL (0,62 mmol/L) par mois et ne pas dépasser 2 g/dL/mois (1,25 mmol/L) afin de minimiser les risques d'hypertension.
Chez les patients en insuffisance rénale chronique, la concentration d’hémoglobine d’entretien ne doit pas dépasser la limite supérieure de l’intervalle des concentrations d’hémoglobine telle que recommandée dans la rubrique 4.2. Dans les études cliniques, un risque augmenté de décès et d’évènements cardiovasculaires graves a été observé lorsque les ASE étaient administrés afin d’obtenir un taux d’hémoglobine supérieur à 12 g/dL (7,5 mmol/L).
Les études cliniques contrôlées n’ont pas montré de bénéfices significatifs attribuables à l’administration d’époétines lorsque la concentration d’hémoglobine est augmentée au-delà du taux nécessaire pour contrôler les symptômes de l’anémie et pour éviter une transfusion sanguine.
La prudence s’impose en cas d’augmentation de dose d’EPREX chez les patients ayant une insuffisance rénale chronique car des doses cumulatives d’époétine élevées peuvent être associées à un risque accru de mortalité et d’évènements graves cardiovasculaires et cérébrovasculaires. Chez les patients ayant une réponse faible aux époétines, d’autres facteurs expliquant la faible réponse devront être considérées (voir rubriques 4.2 et 5.1).
Les patients en insuffisance rénale chronique traités par époétine alfa par voie sous-cutanée devront être suivis régulièrement afin de rechercher une perte d’efficacité, définie par l’absence de réponse ou une diminution de la réponse au traitement par époétine alfa chez des patients antérieurement répondeurs à ce traitement. Cette perte d’efficacité est caractérisée par une diminution constante de l’hémoglobine malgré l’augmentation des doses d’époétine alfa (voir rubrique 4.8).
Certains patients ayant un intervalle d’administration d’époétine alfa plus long (supérieur à une semaine) peuvent ne pas maintenir un taux d’hémoglobine approprié (voir rubrique 5.1) et peuvent nécessiter une augmentation de la dose d’époétine alfa. Les taux d’hémoglobine doivent être surveillés régulièrement.
Des thromboses de la fistule artério-veineuse sont survenues chez les patients hémodialysés, particulièrement chez ceux ayant une tendance à l'hypotension ou présentant des complications au niveau de leur fistule (par exemple sténoses, anévrysmes, etc.). Une révision précoce de la fistule artério-veineuse et une prophylaxie anti-thrombotique par administration d’acide acétylsalicylique, par exemple, sont recommandées chez ces patients.
Une hyperkaliémie a été observée dans des cas isolés, bien que le lien de causalité n’ait pas été établi. L'ionogramme sanguin doit être surveillé chez les patients insuffisants rénaux chroniques. En cas d'hyperkaliémie ou d'augmentation de la kaliémie, l'arrêt d'époétine alfa jusqu'à correction du taux sérique de potassium peut être envisagé en plus du traitement approprié de l’hyperkaliémie.
Lors d'un traitement par époétine alfa, l'augmentation de l'hématocrite rend souvent nécessaire d'augmenter les doses d'héparine pendant l'hémodialyse. L’obstruction du système de dialyse peut survenir si l'héparinisation n'est pas optimale.
D'après les données disponibles à ce jour, la correction de l'anémie par époétine alfa chez les patients adultes insuffisants rénaux non encore dialysés n'accélère pas l'évolution de l'insuffisance rénale.
Traitement des patients ayant une anémie induite par la chimiothérapie :
Chez les patients atteints d’un cancer traités par époétine alfa, les taux d'hémoglobine doivent être régulièrement mesurés jusqu'à ce qu'un taux stable soit atteint, puis périodiquement ensuite.
Les époétines sont des facteurs de croissance qui stimulent essentiellement la production de globules rouges. Des récepteurs à l’érythropoïétine peuvent être présents à la surface de diverses cellules malignes. Comme pour tout facteur de croissance, la possibilité que les époïétines puissent stimuler la croissance des tumeurs ne peut pas être exclue.
Le rôle des ASE sur la progression tumorale ou la réduction de la survie sans progression ne peut être exclu. Dans des études cliniques contrôlées, l’utilisation d’époétine alfa et d’autres ASE a été associée à une diminution du contrôle loco-régional ou à une diminution de la survie globale :
- une diminution du contrôle loco-régional chez des patients atteints d’un cancer de la tête et du cou avancé recevant une radiothérapie lorsque l’administration visait un taux d’hémoglobine supérieur à 14 g/dL (8,7 mmol/L),
- un raccourcissement de la survie globale et une augmentation du nombre de décès attribués à la progression de la maladie à 4 mois chez des patients atteints d’un cancer du sein métastatique recevant une chimiothérapie lorsque l’administration visait un taux d’hémoglobine de 12 à 14 g/dL (7,5 à 8,7 mmol/L),
- une augmentation du risque de décès lorsque l’administration visait un taux d’hémoglobine de 12 g/dL (7,5 mmol/L) chez des patients ayant une maladie maligne active ne recevant ni chimiothérapie ni radiothérapie. Les ASE ne sont pas indiqués pour une utilisation dans cette population de patients,
- une augmentation observée de 9 % du risque de progression de la maladie ou de décès dans le bras associant époétine alfa à des traitements standards d’après les résultats d’une analyse primaire et une augmentation du risque de 15 % ne pouvant être statistiquement exclu chez les patients recevant une chimiothérapie pour un cancer du sein métastatique, lorsque l’administration visait un taux d’hémoglobine compris entre 10 et 12 g/dL (6,2 à 7,5 mmol/L).
Au vu des informations ci-dessus, dans certaines situations cliniques, la transfusion sanguine devrait être le traitement privilégié de l’anémie des patients atteints de cancer. La décision d’administrer une érythropoïétine recombinante doit être déterminée sur une évaluation du bénéfice/risque prenant en compte l’avis du patient dans son contexte clinique spécifique. Les facteurs à considérer dans cette évaluation doivent inclure le type de tumeur et son stade, le degré de l’anémie, l’espérance de vie, l’environnement dans lequel le patient est traité et la préférence du patient (voir rubrique 5.1).
Lorsque l'on évalue le caractère approprié d'un traitement par époétine alfa chez les patients atteints d’un cancer recevant une chimiothérapie (patient à risque d'être transfusé), il faut tenir compte du fait que l'apparition des globules rouges suit l'administration de l’ASE avec un délai de 2 à 3 semaines.
Patients adultes en chirurgie participant à un programme de transfusions autologues différées
Toutes les mises en garde et précautions particulières d'emploi associées à un programme de transfusions autologues différées doivent être respectées, en particulier le remplacement en routine du volume prélevé.
Patients devant avoir une chirurgie orthopédique majeure programmée
Les bonnes pratiques de gestion du sang doivent toujours être appliquées dans le cadre péri-opératoire. Les patients devant bénéficier d'une chirurgie orthopédique majeure programmée, doivent recevoir une prophylaxie antithrombotique appropriée, dans la mesure où des événements thrombotiques et vasculaires peuvent survenir chez ces patients, particulièrement chez ceux ayant une pathologie cardio-vasculaire sous-jacente. De plus, des précautions particulières doivent être prises chez les patients à risque de développer des thromboses veineuses profondes. Enfin, chez les patients ayant un taux initial d'hémoglobine supérieur à 13 g/dL, la possibilité que le traitement par époétine alfa soit associé à un risque accru d'événements thrombotiques/vasculaires post-opératoires, ne peut être exclue. En conséquence, l'époétine alfa ne doit pas être utilisée chez les patients qui ont un taux d'hémoglobine initial supérieur à 13 g/dL.
Excipients
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose, c’est-à-dire qu’il est essentiellement « sans sodium ».
Condition de prescription
prescription initiale hospitalière annuelle
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Important
Présentation : 6 seringue(s) préremplie(s) en verre de 0,5 ml avec aiguille(s)
Prix : 54.84
Taux de remboursement : 65%
Titulaire : JANSSEN CILAG