LIDBREE 42 mg/mL, gel intra-utérin
Classe médicamenteuse
Anesthésiques ; Anesthésiques locaux | Code ATC : N01BB02
Composition
Lidocaïne ............................................................................................................................. 42 mg
Pour un mL.
Excipients à effet notoire :
Chaque mL de gel contient 284 mg de ricinoléate de macrogolglycérol (huile de ricin polyoxyéthylénée) et jusqu’à 28 microgrammes de butylhydroxytoluène (E 321).
Indications thérapeutiques
Lidbree est indiqué dans l’anesthésie locale des douleurs aiguës modérées lors des procédures cervicales et intra-utérines, chez les femmes adultes et les adolescentes âgées de 15 ans et plus. Voir rubrique 5.1.
Posologie et mode d'administration
Posologie
Procédures cervicales
Appliquer une couche épaisse 2 à 3 mL de gel sur l’orifice cervicale et 3 mL à l’intérieur ducanal cervical en utilisant l’applicateur stérile, 5 minutes avant le début de la procédure.
Procédures intra-utérines
À l’aide de l’applicateur stérile, appliquer 1 à 2 mL sur la lèvre antérieure du col et 2 à 3 mL dans le canal cervical. Attendre 2 minutes pour l’apparition de l’effet anesthésique au niveau du méat interne. Insérer ensuite l’applicateur dans la cavité utérine et injecter 3 à 5 mL, 5 minutes avant la procédure. L’applicateur est gradué en centimètres. Un volume plus petit peut être administré, p. ex. chez les patientes nullipares, si la patiente présente une gêne avant l’administration de la totalité du volume. La dose intra-utérine à appliquer au cours d’une seule administration ne doit pas dépasser un volume total de 10 mL.
Population pédiatrique âgée de 15 ans et plus
Chez les adolescentes de faible poids corporel, inférieur à 30 kg, la dose doit être proportionnellement réduite et une dose unique ne doit pas dépasser la dose maximale recommandée par voie parentérale (6 mg/kg de chlorhydrate de lidocaïne, correspondant à 5,2 mg/kg de lidocaïne base dans Lidbree, c’est-à-dire 1,2 mL pour 10 kg de poids corporel). Chez les adolescentes ayant un poids de 30 kg, la dose maximale totale de Lidbree est de 3,6 mL.
La sécurité et l’efficacité de Lidbree chez les jeunes filles âgées de moins de 15 ans n’ont pas été établies. Lidbree ne doit pas être utilisé chez les enfants âgés de moins de 15 ans en raison de problèmes de sécurité (voir rubriques 4.4 et 5.1).
Patientes âgées
Aucune réduction de dose n’est nécessaire les patientes âgées (voir rubrique 5.2).
Insuffisance hépatique
En cas d’administration unique, il n’est pas nécessaire de réduire la dose chez les patientes ayant une altération de la fonction hépatique (voir rubrique 5.2).
Insuffisance rénale
Une réduction de dose n’est pas nécessaire chez les patientes ayant une insuffisance rénale.
Mode d’administration
Utilisation par voies cervicale et intra-utérine strictes.
Au moment de l’administration, Lidbree doit être liquide. S’il s’est transformé en gel, il faut le mettre au réfrigérateur jusqu’à ce qu’il redevienne liquide. La bulle d’air visible dans la seringue se déplacera si l’on incline la seringue.
Préparer le produit par étapes et appliquer le liquide visqueux en utilisant l’applicateur stérile fourni dans l’emballage :
1) Incliner la seringue et vérifier son aspect. Si le produit est sous forme liquide et prêt à l’emploi, la bulle d’air dans la seringue se déplacera lors de l’inclinaison de la seringue. Si la bulle d’air ne bouge pas, cela signifie que le produit s’est transformé en gel – dans ce cas, mettre la seringue au réfrigérateur jusqu’à ce que le produit redevienne liquide.
2) Connecter le piston et l’applicateur à la seringue et s’assurer qu’ils sont solidement attachés.
![]()
3) Expulser la bulle d’air et remplir l’applicateur de gel en enfonçant prudemment le piston de la seringue.
4) Utiliser la graduation en centimètres de l’applicateur pour préparer l’administration du gel Lidbree.
Lorsque l’applicateur est en place, 8,5 mL de gel peuvent être délivrés par la seringue. Un mL contient 42 mg de lidocaïne. Appliquer le gel par étapes (1 à 3) comme illustré sur le dessin.
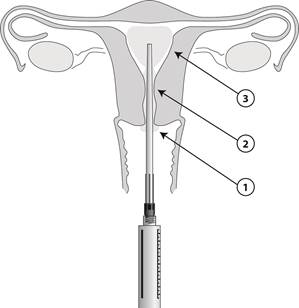
Voie d'administration
endocervicale;intra-utérine
Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
Mise en garde et précautions d'emploi
Voie cervicale et intra-utérine stricte. Des symptômes aigus de toxicité liée à l’anesthésique local et des complications emboliques engageant le pronostic vital peuvent survenir si le liquide visqueux thermogélifiant est accidentellement injecté par voie intravasculaire (voir rubrique 4.9 pour le traitement des réactions toxiques systémiques). L’administration accidentelle par d’autres voies parentérales peut conduire à une toxicité tissulaire locale.
En cas de difficultés d’insertion de contraceptifs intra-utérins et/ou de saignement ou douleur inhabituels survenant pendant ou après l’insertion, un examen clinique et une échographie doivent être immédiatement réalisés afin d’exclure une perforation du col ou du corps de l’utérus, car en présence d’anesthésiques topiques efficaces, la patiente pourrait ne pas réagir à la douleur en cas de perforation.
Certaines patientes nécessitent une attention particulière :
- Patientes ayant un bloc auriculo-ventriculaire partiel ou complet – car les anesthésiques locaux peuvent inhiber la conduction myocardique.
- Les patientes traitées par des antiarythmiques de classe III (p. ex. amiodarone) doivent faire l’objet d’une surveillance étroite et une surveillance ECG doit être envisagée chez ces patientes car les effets cardiaques peuvent être additifs.
- Patientes atteintes de porphyrie aiguë. La lidocaïne est probablement porphyrinogénique et elle doit être prescrite aux patientes atteintes de porphyrie aiguë uniquement en cas d’indications urgentes ou impérieuses. Des précautions appropriées doivent être prises pour toutes les patientes atteintes de porphyrie.
- Patientes en mauvais état général.
Population pédiatrique
Lidbree ne doit pas être administré sur les muqueuses des enfants âgés de moins de 15 ans, car les concentrations plasmatiques de lidocaïne pourraient dépasser le seuil de toxicité (voir rubrique 5.1).
Excipients
Ce médicament contient du ricinoléate de macrogolglycérol (huile de ricin polyoxyéthylénée) et du butylhydroxytoluène (E 321).
Le ricinoléate de macrogolglycérol peut provoquer de graves réactions allergiques.
Le butylhydroxytoluène (E 321) peut provoquer une irritation des muqueuses.
Condition de prescription
liste II
Groupe générique
Non renseigné
Forme pharmaceutique
Non renseigné
Divers
Service Médical Rendu (SMR) : Non disponible
Présentation : 1 seringue préremplie copolymère de cyclooléfines de 10 mL avec applicateur stérile polypropylène embout Luer-Lock
Prix : non disponible
Taux de remboursement : 0%
Titulaire : GEDEON RICHTER